临床前动物实验(包括免疫实验和攻毒实验)阶段不需太长时间,其中攻毒实验**短1个月即可。但这依赖于动物产生免疫的情况,是否产生了很好的中和抗体。由于目前人类能够进行特异性测定的主要是抗体,其他的(比如细胞因子、体细胞的免疫反应等)很难进行***准确评价。是否简化、如何简化,取决于前期是否有扎实充分的研究基础。做动物实验不仅是评价安全有效以及能否上临床,更要评价其对人是否会有效?有诸多问题值得注意,比如攻毒实验需要用的疫苗免疫剂量是多少?佐剂是什么?什么时间攻毒?如何对人进行注射?注射方式以及剂量、次数是多少?等等。中成药临床前动物实验指导原则;海南临床前动物实验研究
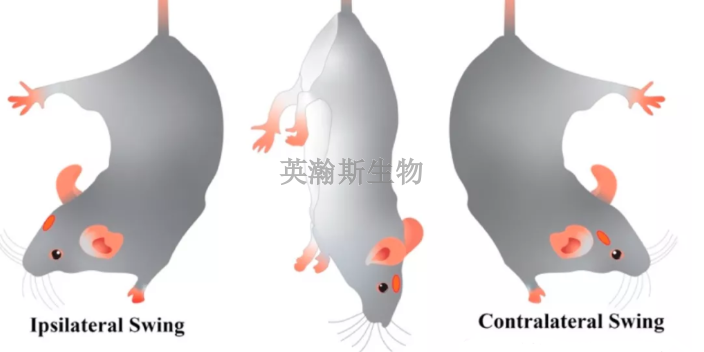
临床前动物实验方案尽可能模拟临床设计和使用。应当确认在输送、植入或使用器械中的所有步骤,并制定每一个步骤的可接受标准。建议对每个验收标准应用半客观的评定量化表(例如李克特量表,Likert scale)。如果器械与辅助设备一同输送或使用,则可接受标准应包含评估系统相容性的要素。评级标准应当囊括从器械准备到放置或使用乃至取回和重新放置过程中的所有步骤。如果器械通过手术放置,则应描述器械从进入体壁到比较终器械操作期间的所有步骤。广西推荐的临床前动物实验研究生物药临床前动物实验包括哪些?
临床前动物实验的标准操作规程以及实验计划和实验方案制定:医疗器械的安全性评估通常基于所提供有效科学证据的动物实验研究,应具有适当的标准操作规程,以确保数据的质量和完整性。研究机构应当制定与其业务相适应的标准操作规程。关于需要制定的标准操作规程可参考《药物非临床研究质量管理规范》第七章的合计15项条款。建议临床前动物实验研究包括适当的控制措施以尽量减少实验的变异性和差错。这样的措施包括但不限于在试验过程中尽量减少影响实验动物的因素。
从临床前动物实验到临床试验,路在何方?这样的悲剧也揭示了一个令人不安的事实,人们对人类免疫系统的认识还存在很多盲点,而动物实验和临床试验也经常出现相左的结果。那么,我们现有的临床试验体系是否安全可靠?为了防止这样的悲剧再次发生,应该如何设计临床试验?从动物实验到人体试验,路该如何走?ESG根据调查结果并普遍征询了**意见后提出22条关于如何改善初次用于人体药物的Ⅰ期临床试验安全性建议。主要关注如何计算初次应用的药物剂量、如何给药;不同研究组织和医药公司应共享有关药物临床试验不良反应(特别是未发表的)、失败的药物试验等资料;特殊药物,例如作用于人体生理过程的生物药物,在进行研究之前应征求单独**的意见等。英瀚斯专业做化学药药临床前动物实验外包。

申请人应尽临床前动物实验的可能通过初步研究(如实验室研究等)来验证所确定的风险控制措施的有效性,只有在实验室研究不足时,才能通过动物实验进行进一步验证。动物实验数据可作为风险/收益分析的支持数据。1.可行性研究:可行性研究是指在产品设计和开发阶段,为确认/验证产品的工作原理、作用机理、设计、可操作性、功能性、安全性等方面,或识别新的意外风险而进行的研究。2.安全性研究:申请人采取风险控制措施后,可通过动物实验对部分产品的安全性进行适当评价。3.有效性研究:尽管某些医疗器械在动物和人类之间的有效性可能存在一些差异,但合理设计的动物实验可以支持产品的有效性(包括性能和操作)。中成药临床前动物实验外包;天津专注临床前动物实验
中成药临床前动物实验中心;海南临床前动物实验研究
临床前动物实验研究监测②中期观察:在动物从初始手术过程中恢复,监测器械相关风险期间,建议每天至少在喂食时间监测两次,以便在活动时观察它们。同时,建议咨询兽医并制定体重监测计划。应考虑将体重评分作为定期观察动物的辅助手段。如果研究涉及收集临床生化检测数据或更先进的诊断,建议制定标准操作规程以便在需要时指定一种不***械的化学干预方法。③终期研究期:建议实验方案应包括终期研究的细节,并包括检查、采集和组织处理的所有方法。具体方案应包括终点检验的方法、完成***放射线分析和成像分析的陈述(如果适用)、确定**终体重和机体评分的方法。④尸体解剖和评估:不良事件可能会出现在临床或亚临床期。因此,建议在研究中纳入***的系统性尸检,包括组织收集和保存,以进行组织病理学检查。所得信息可协助确定不良事件与器械的相关性。海南临床前动物实验研究