综合腺相关病毒AAV制备的三个工艺阶段介绍,可以看出下游处理可以占病毒生产总成本的很大一部分,而且难度也是非常大,尤其是纯化过程。原因之一是由于有超过100种不同血清型的变体AAV衣壳,不同血清型的AAV蛋白存在差异。因此,各种血清型的表面特性增加AAV纯化难度。原因之二是:针对工艺和产品相关的杂质(包括宿主细胞物质,DNA和空衣壳),缺乏一个有效和可重复的平台方法,尤其是来从空衣壳中分离出完整的衣壳。为了解决以上问题,国内外大的药企公司都致力于纯化新产品的开发,以期达到:(1)实现病毒颗粒的分离(2)减少产品相关杂质(3)保持效力和产量的目标。SAN HQ用量是Benzonase用量的1/3-1/4,酶用量更少,成本更低、工艺更简单。河南高盐条件高盐核酸酶70921-160

Mayer等(2023)以measles virus(麻疹病毒,MV)为例,评估了四种不同核酸酶(BenzonaseTM、DeneraseTM、M-SAN HQ中盐核酸酶及SAN HQ高盐核酸酶)对于染色质DNA去除的效果。Vero细胞通过微载体贴壁培养来生产麻疹病毒MV,72hr后收获上清液,使用3µm cellulose filter(Sartorius)过滤后分装多份,置于-80℃保存便于后续使用。在解冻后的上清中调节对应盐浓度,并加入50 U/ml核酸酶,37℃孵育2hr进行消化,消化后留样;将消化后上清液过Capto Core 700 (Cytiva)柱子,收集流穿液,之后洗杂、洗脱,并分别留样。通过SDS-PAGE分析发现,相比Benzonase等传统核酸酶,在生理盐条件下M-SAN HQ中盐核酸酶更高效将染色质DNA剪切成更小片段,甚至将核小体DNA剪切更彻底。陕西ArcticZymes高盐核酸酶70921-202在符合ISO13485:2016体系基础上,增加了cGMP相应要求。
SAN HQ高盐核酸酶发挥酶活性的条件比较广。例如,该酶适宜的盐浓度(NaCl)范围是400mM-600mM,能耐受高达1M NaCl浓度。适宜反应温度为25℃-37℃,能耐受4℃-38℃。Mg2+浓度大于1mM即可,在5-20mM范围即可表现更高活性。跟全能核酸酶类似,SAN HQ高盐核酸酶也是一款碱性核酸酶,其适宜pH为8.0-8.9,能耐受6.8-9.5。为了达到更高酶活性,可以通过调节pH实现。鉴于SAN HQ的耐受性,可以用于很多应用,如大规模生产、蛋白纯化、蛋白组学等。
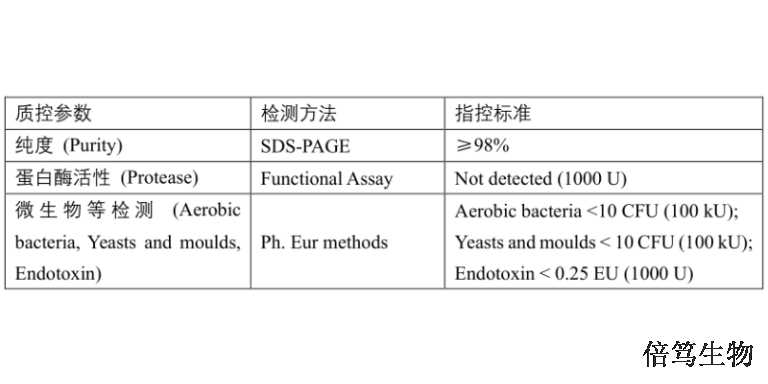
ArcticZymes厂家对盐活性核酸酶系列产品(Salt Active Nucleases,SANs)的生产及质控,在符合ISO13485:2016体系基础上,增加了cGMP质控标准,如microbes、endotoxin、蛋白酶等,符合USP-EP要求。厂家提供HQ级别和GMP级别的SAN HQ高盐核酸酶和M-SAN HQ中盐核酸酶,从成本角度分别满足临床前和早期临床阶段、商业化大规模生产阶段的需求;且GMP级SAN HQ高盐核酸酶已完成在FDA的药物主文件(Drug Master File, DMF)申报备案,助力加快药物申报流程。在生物制品生产,如AAV载体及腺病毒载体疫苗生产中,宿主细胞DNA残留是关键质量参数之一。
有研究发现,杆状病毒表达载体体系BEV生产的rAAV发生了与293生产体系不同的衣壳蛋白翻译后修饰(post-translationalmodifications,PTMs)。这一差异是否会影响载体趋向性和转导效率还需要进一步验证。除此之外,杆状病毒多重infection会导致载体蛋白VP1、VP2和VP3比例不一致。尽管如此,BEV/Sf9系统仍然是一种颇有吸引力的大规模临床级载体生产策略。随着以后对基因药物需求的增加,AAV载体的需求量也会与日俱增,而BEV系统能够降低AAV的成本,未来还是很有发展潜力的。SAN HQ高盐核酸酶促进残留DNA的消化,有助于符合FDA要求。河北基因药物生产用高盐核酸酶
SAN HQ终产品经过0.22 µm过滤除菌;河南高盐条件高盐核酸酶70921-160
一般来说,生物生产工艺用的核酸酶以BenzonaseTM(BenzonaseTM是Merck的注册商标)为主,能高效降解任何形式(双链、单链、线状、环状)的DNA和RNA。该酶来自于大自然界普遍存在的S.Marcescen,通过E.coli发酵生产得到。该酶的适宜反应条件是低盐浓度范围(<100mM盐浓度),且酶活随着盐浓度上升而下降,在300mM盐浓度时酶活几乎丧失。对于细胞基因药物常用的两种病毒载体LV和AAV,LV由于含有脂包膜结构一般都在生理盐条件下存在,而AAV在高盐条件下不易团聚、更稳定。而在生理盐浓度及更高浓度条件下,Benzonase活性受到抑制。河南高盐条件高盐核酸酶70921-160
上海倍笃生物科技有限公司在同行业领域中,一直处在一个不断锐意进取,不断制造创新的市场高度,多年以来致力于发展富有创新价值理念的产品标准,在上海市等地区的医药健康中始终保持良好的商业口碑,成绩让我们喜悦,但不会让我们止步,残酷的市场磨炼了我们坚强不屈的意志,和谐温馨的工作环境,富有营养的公司土壤滋养着我们不断开拓创新,勇于进取的无限潜力,上海倍笃生物科技供应携手大家一起走向共同辉煌的未来,回首过去,我们不会因为取得了一点点成绩而沾沾自喜,相反的是面对竞争越来越激烈的市场氛围,我们更要明确自己的不足,做好迎接新挑战的准备,要不畏困难,激流勇进,以一个更崭新的精神面貌迎接大家,共同走向辉煌回来!
ArcticZymes Technologies成立于20世纪80年代后期,致力于从海洋生物中识别新...
【详情】核酸酶活性受到很多因素影响,如盐浓度、pH、底物、温度等。因此,不同客户、不同项目中核酸酶的使用条件...
【详情】近年来,AAV在cancer疾病的医治中显示出巨大的价值。AAV作为基因药物的载体已在肺、肝、眼、脑...
【详情】ArcticZymes Technologies于2017年推出了SAN HQ高盐核酸酶及其对应的S...
【详情】近年来,AAV在cancer疾病的医治中显示出巨大的价值。AAV作为基因药物的载体已在肺、肝、眼、脑...
【详情】离子交换层析 (IEC) 是一种简单、通用且经济高效的技术,已成为许多载体纯化的关键步骤。IEC分为...
【详情】通过三质粒瞬转体系生产病毒载体,会引入宿主细胞DNA残留(HCD)、蛋白残留(HCP)、工艺杂质(如...
【详情】通过三质粒瞬转体系生产病毒载体,会引入宿主细胞DNA残留(HCD)、蛋白残留(HCP)、工艺杂质(如...
【详情】综合腺相关病毒AAV制备的三个工艺阶段介绍,可以看出下游处理可以占病毒生产总成本的很大一部分,而且难...
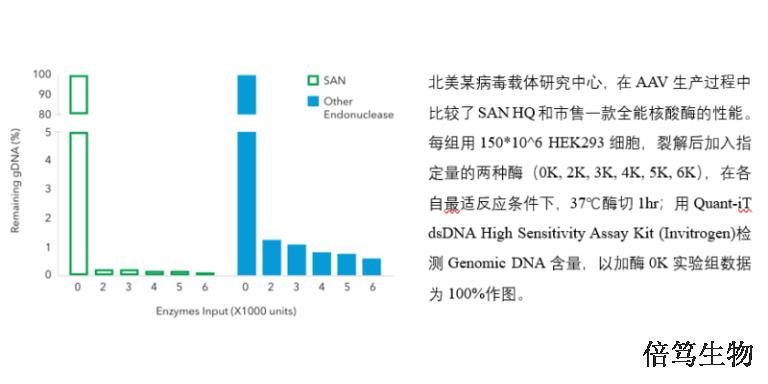
【详情】一个美国客户做了对照实验,比较Benzonase和SAN HQ高盐核酸酶纯化病毒载体的效率。实验设计...
【详情】