染色质免疫沉淀(ChromatinImmunoprecipitation,ChIP)是研究体内蛋白质与DNA相互作用的一种技术。ChIP实验通过使用特异性抗体与染色质相互作用,并通过免疫沉淀的方式,将特定蛋白质与染色质结合的区域沉淀下来,在全基因组水平研究生命体组织或细胞内蛋白质与DNA相互作用。ChIP常应用于研究转录因子与启动子的互作。ChIP实验原理:在活细胞状态下,通过甲醛固定DNA-蛋白质复合物后,采用微球菌核酸酶随机切断DNA,形成一定长度范围内的染色质小片段,通过抗原-抗体特异性结合反应富集、沉淀这些小片段,然后分离蛋白,纯化DNA,采用PCR或测序检测DNA的序列信息。ChIP实验在解析基因表达调控机制、研究转录因子结合位点等方面具有重要意义。ChIP-qPCR实验流程包括交联细胞、裂解细胞核、切割染色质、免疫沉淀、洗涤、反交联、DNA纯化和QPCR反应等。新疆chromatin免疫沉淀ChIP
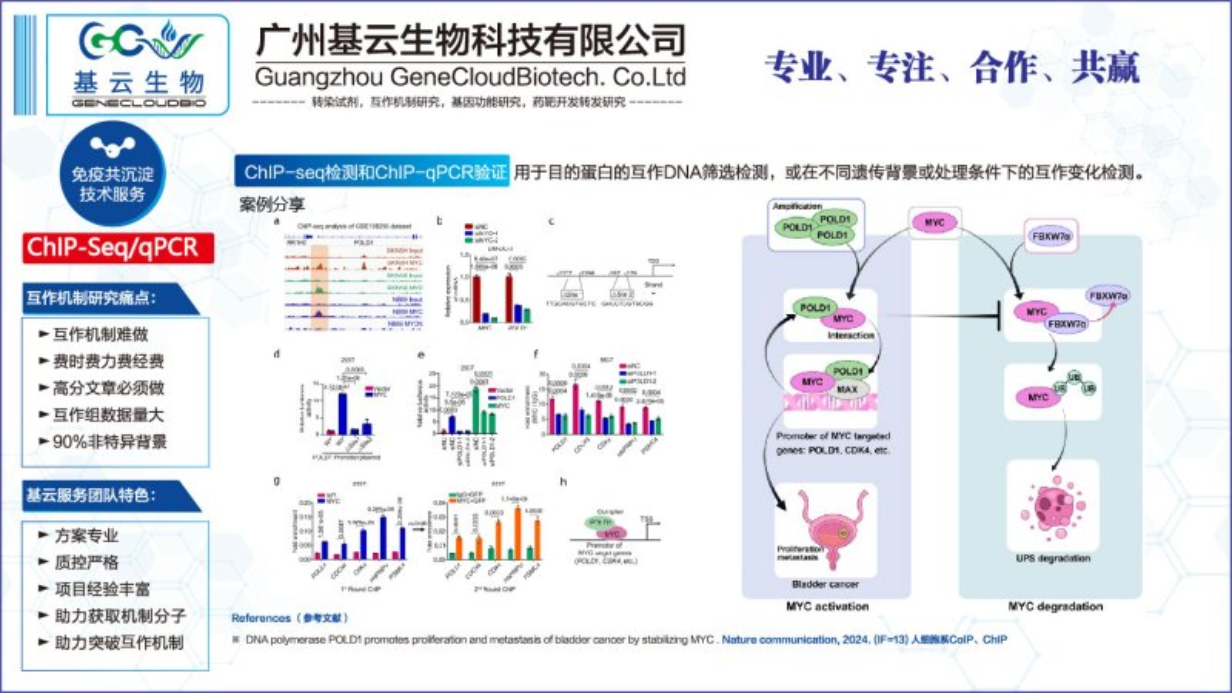
ChIP-qPCR和ChIP-seq实验在多个方面存在异同点。首先,在实验流程上,两者都包含染色质免疫沉淀这一关键步骤,用于富集与特定蛋白质结合的DNA片段。然而,在后续的检测方法上,它们有所不同。ChIP-qPCR采用实时荧光定量PCR技术对这些片段进行定量检测,适用于已知蛋白质与靶序列相互作用的研究。而ChIP-seq则结合了高通量测序技术,能够在全基因组范围内检测与特定蛋白质结合的DNA区域,适用于未知靶序列的探索。其次,在分辨率上,ChIP-seq具有更高的分辨率,能够提供完整、高分辨率的结合信息,绘制出转录因子等蛋白质在全基因组范围内的结合位点图谱。而ChIP-qPCR的分辨率相对较低,通常只能针对已知基因或基因区域进行分析。另外,在应用范围上,ChIP-seq在探索转录调控网络、表观遗传机制等领域具有更广泛的应用价值。而ChIP-qPCR则更适用于验证特定转录因子与基因启动子的结合等具体作用机制的研究。综上所述,ChIP-qPCR和ChIP-seq在实验流程、分辨率和应用范围上存在异同点,研究者应根据具体需求选择合适的技术方法。贵州染色体蛋白相互作用ChIPChIP实验是基于抗原-抗体反应的特异性,结合染色质的结构特性,从而研究蛋白质与DNA在染色质上的相互作用。
染色质免疫沉淀(ChIP)实验常见的应用场景。转录因子结合位点分析:ChIP常用于鉴定转录因子在基因组上的结合位点,助于理解转录调控机制和基因表达模式。染色质修饰研究:通过ChIP实验,可以研究染色质上特定修饰(如甲基化、乙酰化、磷酸化等)的分布和动态变化,以及这些修饰如何影响基因表达。基因表达调控研究:ChIP可用于研究基因启动子区域或增强子区域的蛋白质结合情况,揭示基因表达调控的机制。疾病发生机制的研究:ChIP技术可以帮助研究人员了解疾病相关基因在染色质上的调控机制,如AI、神经性疾病等。药物靶点发现:ChIP可用于筛选和验证药物作用的靶点,为药物研发提供依据。基因组功能注释:通过ChIP技术,可以对基因组进行功能注释,识别具有特定功能的基因组区域。
ChIP实验(染色质免疫沉淀实验)的一般实验流程主要包括以下步骤:细胞的准备及固定:细胞在培养皿中生长到适当密度后,进行交联处理以固定细胞内的蛋白质和DNA复合物。染色质超声断裂:加入裂解液裂解细胞膜和核膜,释放染色质。随后进行超声处理,将染色质断裂成适当大小的片段,有利于后续的免疫沉淀。免疫沉淀:使用特异性抗体与目标蛋白质(如转录因子)结合,形成免疫复合物。通过磁珠或琼脂糖珠等固相支持物捕获这些复合物,从而富集与目标蛋白质结合的DNA片段。洗脱和解交联:洗涤去除非特异性结合的杂质后,进行解交联处理,使蛋白质与DNA之间的交联键断裂,释放DNA片段。DNA纯化:通过酚/氯仿抽提、乙醇沉淀或硅胶柱纯化等方法纯化DNA片段。数据分析:纯化后的DNA片段可以进行PCR、测序或芯片分析等,以确定目标蛋白质在基因组上的结合位点。此外,在实验过程中还需要注意一些细节,如避免DNA污染、优化超声条件、选择合适的抗体等。同时,设置适当的对照实验也是确保结果准确性的重要环节。ChIP-qPCR实验是一种结合染色质免疫沉淀(ChIP)与实时荧光定量PCR(qPCR)的技术。
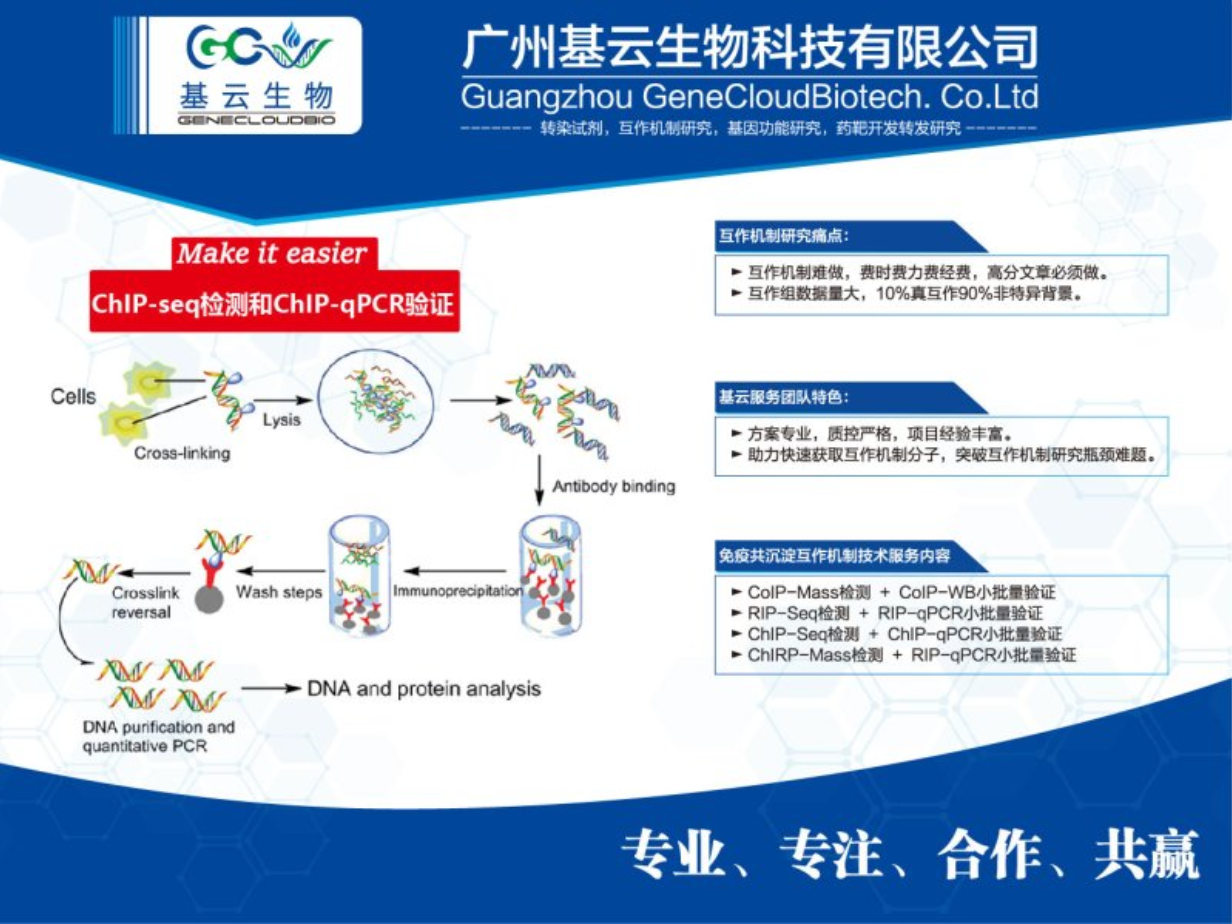
在染色质免疫沉淀(ChIP)实验过程中,可能遇到的问题及其解决方案(一)。染色质裂解不完全:可能导致DNA与蛋白质之间的结合不稳定,影响实验结果。解决方案:优化裂解液配方、调整裂解时间和温度,以及确保使用新鲜且状态良好的细胞或组织样品。抗体特异性不足:若抗体不能特异性地识别目标蛋白质,可能导致非特异性结合和假阳性结果。解决方案:选择特异性好、质量可靠的抗体,并进行抗体验证实验。免疫沉淀效率低:可能是由于抗体与染色质结合不充分或洗涤步骤不当导致的。解决方案:增加抗体用量、优化免疫沉淀时间和温度,以及调整洗涤条件和次数。在进行更大规模的ChIP-seq实验之前,ChIP-qPCR可以作为初步筛选或验证特定蛋白质与DNA结合位点的有效工具。中国香港chromatin蛋白相互作用ChIP
ChIP-qPCR和ChIP-seq在实验流程、分辨率和应用范围上存在异同点,应根据具体需求选择合适的技术方法。新疆chromatin免疫沉淀ChIP
Q:ChIP-Seq和ChIP-qPCR有何异同?A:染色质免疫共沉淀(ChIP)所获得的DNA产物,在ChIP-Seq中通过高通量测序的方法,在全基因组范围内寻找目的蛋白(转录因子、修饰组蛋白)的DNA结合位点片段信息;ChIP-qPCR需要预设待测的目的序列,针对目的序列设计引物,以验证该序列是否同实验蛋白结合互作。
Q:染色质片段大小在哪个范围比较合适?A:对于ChIP-seq,片段在200-500bp左右是合适范围;对于ChIP-qPCR,片段在200-800bp左右适宜。
Q:植物样本处理和动物组织/细胞有何区别?A:植物组织由于细胞壁、气腔等结构的存在,会给交联缓冲液的作用带来困难,因此相对于动物组织/细胞来说,往往需要在抽真空条件下进行交联,而该步奏是一个需要经验及优化的过程。
Q:ChIP-Seq中的测序DNA样本需要多少产量?A:通常是≥10ng。
Q:ChIP风险如果判断A:ChIP实验以标签来判断实验风险,重组标签的转录因子>内源转录因子>组蛋白;当以重组蛋白作为靶蛋白时,重组蛋白同内源蛋白可能存在结合活性、结合位点差异;以标签抗体进行ChIP时、染色质结合位点本身会被内源蛋白竞争,这些都会影响到ChIP过程的特异性捕获效率。 新疆chromatin免疫沉淀ChIP