脂质体核酸疫苗核酸***剂是一类新兴的药物,显示出***各种疾病的潜力。然而,由于核酸是多价阴离子和高度亲水分子,它们几乎不被细胞吸收。它们也很容易被血液中的核酸酶降解。因此,它们需要一种传递载体才能进入细胞并发挥作用。LNP载体是核酸类药物的成功载体之一。核酸药物Patisiran(ONPATTRO)是一种在LNPs中配方的siRNA,用于减少肝脏中甲状腺素转运蛋白的形成,**近获得FDA批准用于***遗传性甲状腺素转运介导的淀粉样变性。它是**早获批的siRNA药物,也是**早的lnp配方核酸药物,标志着核酸***学发展的一个重要里程碑。COVID-19mRNA疫苗中的LNPs。LNPs的***成功应用是辉瑞/BioNTech和莫当纳**近批准的两种COVID-19信使RNA(mRNA)疫苗的递送载体,这两种疫苗的开发速度****,在疾病预防方面显示出显着的效果。疫苗将编码SARS-CoV-2刺突蛋白的mRNA送入宿主细胞细胞质;mRNA被翻译成刺突蛋白,刺突蛋白作为抗原,导致对病毒产生免疫反应。两种mRNA疫苗的脂质纳米颗粒的组成非常相似。脂质体的缓释作用可以减少给药频率。长循环脂质体载药核酸

脂质体制备方法:薄膜⽔化法薄膜⽔化法是⼀种传统的技术,有利于装载亲脂***物。薄膜是通过在真空条件下烧瓶旋转过程中使脂质溶剂溶液蒸发⽽形成的。MLVs悬浮液可以通过加⼊⽔溶液⽔化脂膜得到。进⼀步缩⼩粒径可获得SUV,在脂质体形成过程中或形成脂质体后,可分别被动或主动装载原料药。AmBisome,Visudyne,andShingrix的商业产品都采⽤这种⽅法制造。例如,Visudyne是通过从⼆氯甲烷中蒸发成分,与乳糖溶液⽔化,均质化,过滤和冻⼲来制造的。佐剂系统as01b是Shingrix产品中的单个⼩瓶,是⼀种基于脂质体的佐剂,含有两种免疫增强剂,QS21(⼀种三萜糖苷,从⽑利纳树的树⽪中纯化)和MPL(3-odesacyl-40-单磷酰脂a)。MPL和其他脂质溶解在有机溶液中并⼲燥。⽔化、减粒径后,加⼊QS21⽔溶液配制。宁夏脂质体载药脂质体质量控制的重要性。
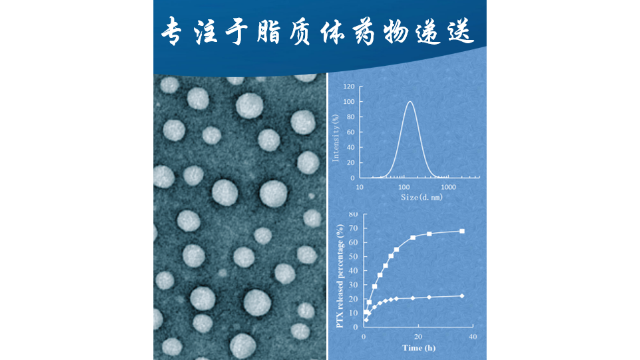
两者都含有一种可电离的脂质,在低pH值下带正电荷(使RNA络合),在生理pH值下为中性(减少潜在的毒性作用并促进有效载荷释放)。它们还含有聚乙二醇化脂质,以减少血清蛋白的抗体结合(调理)和吞噬细胞的***,从而延长体循环。辉瑞公司的阳离子脂质:peg脂质:胆固醇:DSPC的摩尔比为(43:1.6:47:9.4),莫当纳疫苗的摩尔比为(50:1.5:38.5:10)。这些纳米颗粒直径为80 - 100纳米,每个脂质纳米颗粒含有大约100个mRNA分子。ALC-0315(辉瑞)和SM-102 (Moderna)这两种脂质都是叔胺,在低ph下质子化(因此带正电荷)。它们的碳氢链通过可生物降解的酯基连接,在mRNA传递后能够安全***。mRNA疫苗中使用的阳离子脂质含有支链烃链,这优化了非层状相的形成和mRNA的递送效率。peg -脂质均为PEG-2000偶联物。LNPs是在低pH (pH 4.0)条件下制备的,在这种条件下,可电离的脂质带正电,因此它很容易与mRNA形成复合物。微流控装置用于将水中含有mRNA的流与乙醇中含有脂质混合物的流混合。当快速混合时,这两种流的成分形成纳米颗粒,捕获带负电荷的mRNA。
阳离子脂质体的递送的优势各种基于核酸的分子已被研究作为下一代***药物,包括质DNA,反义寡脱氧核苷酸(as-odn),小干扰RNA(siRNA)和微RNA(miRNA)。这些分子共享各种物理化学性质,比化学药物更大,并且携带高度负电荷,限制了它们的细胞递送。因此,核酸疗法要想取得成功,就必须在识别合适的靶蛋白的同时,开发新的递送系统。质粒DNA是**早被认为用于***目的的核酸之一,长期以来一直在基因***的背景下进行研究。在此背景下,研究人员已经将重点放在病毒载体上,它可以赋予高转染效率和基因表达的连续调节。然而,Gelsinger在使用腺病毒载体的临床试验中不幸死亡,让人们意识到病毒材料可能并非完全安全。此外,病毒载体作为候选药物有几个缺点,例如需要为每个靶分子设计载体的不便,以及缺乏关于细胞表达剂量依赖性的知识。载药脂质体可以采用超滤法、凝胶过滤法、低速离心法、透析法等多种方法来纯化。

阳离子脂质体工程系统新脂质的工程化已经被研究作为一种提高核酸递送效率的手段。例如,研究人员合成了胆固醇衍生物阳离子脂质DMHAPC-Chol,并表明其可促进血管内皮生长因子(VEGF)特异性sirna进入肿瘤细胞。在结构上,脂质在其极性氨基头部分具有可生物降解的氨基甲酰基连接剂和羟基乙基。由DMHAPC-Chol和DOPE等摩尔比例组成的阳离子脂质体将VEGFsiRNA传递到A431和MDA-MB-231细胞,并显示出>90%的VEGF蛋白表达的有效沉默。在另一项研究中,开发了一种基于胆固醇的多阳离子脂质体制剂,其中精胺的亲水部分与一个或两个胆固醇残基偶联,用于递送siRNA。由合成的多阳离子脂质和DOPE组成的脂质体可抑制表达EGFP的HEK293细胞中增强的绿色荧光蛋白(EGFP)的表达。除了胆固醇衍生物,基于精氨酸的阳离子脂质也被研究用于siRNA的递送。研究人员合成了由聚l-精氨酸-9偶联聚乙二醇脂质、DOTAP、DOPE和胆固醇组成的聚l-精氨酸脂质衍生物,以增强siRNA的递送。脂质与生物活性小分子(如叶酸)的结合已被研究用于靶向递送核酸。湖北脂质体载药咨询问价
脂质体制备方法:溶剂注射技术。长循环脂质体载药核酸
非病毒载体通常具有比病毒载体更低的转染效率,但由于它们被认为要安全得多,因此已被***研究。纳米颗粒递送系统,其中阳离子脂质纳米颗粒通过核酸的负磷酸基团装载,是一类主要的非病毒载体,显示出高生产力和装载效率。用于携带核酸的纳米颗粒系统在整体上可分为基于脂质或聚合物的纳米颗粒,在与核酸相互作用后,每种纳米颗粒都被称为“脂质复合物”或“多聚体”。这些复合物的细胞递送被认为是通过内吞作用发生的,然后内体逃逸到细胞质中。阳离子脂质体作为核酸的一种传递系统,具有一定的优势。首先,阳离子脂质体在体内给药后是可生物降解的。内源性酶的存在可以分解脂质体的脂质成分。脂质体在各种纳米载体之间****的生物相容性导致在体内研究中使用阳离子脂质体递送各种sirna。脂质组成依赖性的表面电荷密度调节可以控制与带负电的核酸的相互作用力。聚乙二醇化脂质或功能性脂质的包含可以使脂质体的多种表面修饰成为可能。此外,在阳离子脂质体的脂质双层中包含亲脂性化学药物可以提供***药物和***性核酸的共递送。鉴于阳离子脂质体的优势,人们已经研究了阳离子脂质体用于递送各种核酸,如质粒DNA、反义寡核苷酸和siRNA。长循环脂质体载药核酸