脂质体成功降低了绿色荧光蛋白(GFP)的表达,并在H4II-E和HepG2细胞中显示出较低的细胞毒性。在其他研究中,精氨酸衍生物N,N-distearyl-N-methyl-N-2-(N’-arginyl)aminoethylammoniumchloride被用于阳离子脂质体与胆固醇的配制。将这些离子脂质体与c-MycsiRNA络合,并静脉注射给B16F10黑色素瘤小鼠(1.2mg/kg,每天1次,连续3天),导致B16F10**对紫杉醇增敏。另一项研究建议使用精氨酸基DiLA2脂质作为载脂蛋白b特异性siRNA递送的阳离子脂质体组分。经小鼠静脉给药(ED50,0.1mg/kg)后,DiLA2和DOPE制备的阳离子脂质体显示出抑制肝脏载脂蛋白BmRNA表达的潜力。单次全身给药后,在给药后第2天观察到目标mRNA水平的比较大减少(约80%),并且目标mRNA的减少持续到给药后第9天。聚乙二醇在免疫脂质体中起到了重要作用。西安脂质体载药蛋白
5.荧光标记的定量分析:通过测量荧光信号的强度,可以对载药脂质体中药物的含量进行定量分析。这对于确定药物的释放量、药物在体内的浓度以及载药脂质体的稳定性等方面至关重要。荧光标记可以提供一个快速、准确的定量检测方法,为药物输送系统的研究和应用提供了便利。6.探索药物的药代动力学:荧光标记的载药脂质体可以用于研究药物的药代动力学,包括药物的吸收、分布、代谢和排泄过程。通过监测荧光信号的变化,可以跟踪药物在体内的动态变化,从而更好地理解药物的药效学特性。7.提高***效果:荧光标记的载药脂质体还可以用于提高***效果。通过荧光标记,可以实现对***部位的精确定位和定量释放,从而提高药物的局部浓度和***效果,减少对健康组织的损伤和副作用。8.研究药物的靶向性:荧光标记的载药脂质体可以用于研究药物的靶向性。通过将靶向配体或抗体与荧光标记的载药脂质体结合,可以实现对靶向部位的定位和跟踪,从而更好地了解药物的靶向性和作用机制。厦门脂质体载药实验脂质体制备方法:原位制备脂质体。

3脂质体中的相变温度
脂质体中的相变温度是指脂质双分子层中脂质分子从一个状态转变为另一个状态所需的温度。这个温度对于脂质体的性质和功能具有重要作用:1.药物释放控制:脂质体在体内可以通过温度变化来控制药物的释放。例如,如果脂质体的相变温度在人体温度范围内,那么在注射进体内后,脂质体可能会在特定温度下释放药物,这可以用于设计温敏***物输送系统。2.稳定性:相变温度也可以影响脂质体的稳定性。在相变温度以下,脂质体可能会形成固态结构,增加了其稳定性,而在相变温度以上,脂质体可能会转变为液态,导致结构松散和药物释放。3.生物相容性:脂质体的相变温度应当与生物体的温度相匹配,以确保脂质体的生物相容性。如果相变温度太高或太低,可能会对组织或细胞产生不良影响。负载药物的选择:相变温度也可能影响到可负载在脂质体中的药物类型。一些药物可能会干扰脂质体的相变温度,而另一些药物则可能受到相变温度的影响,导致在特定温度下释放。表明脂质体双分⼦层在体温中处于⽆序和药物“漏出”状态。综上所述,脂质体中的相变温度对于药物输送系统的设计和性能调控非常重要,可以影响药物的释放速率、稳定性和生物相容性。
与化学增敏剂共同递送为了增强***活性,研究人员研究了将***siRNA和化学药物共同装载到阳离子脂质体中的共递送方法。例如,将丝裂原活化的蛋白激酶抑制剂PD0325901包封在由N、N-二油基谷酰胺阳离子脂质、DOPE和胆固醇组成的阳离子脂质体中,通过静电相互作用与Mcl-1siRNA络合。在小鼠模型中,瘤内给药这些阳离子脂质体可***抑制**生长。在另一项研究中,开发了基于三叶赖氨酸油酰酰胺的阳离子脂质体,用于共同递送Mcl-1siRNA和***药物亚酰苯胺羟肟酸。与Mcl-1siRNA脂质体或含亚甲基苯胺羟肟酸脂质体的单药***相比,使用载药聚乙二醇化脂质体与Mcl-1siRNA复合物可提高荷瘤小鼠的体内***效果。***,将多柔比星包裹的阳离子脂质体与编码磷酸化缺陷小鼠survivin蛋白的质粒DNA复合,该蛋白是BIRC5基因编码的一种致*蛋白,是凋亡抑制剂家族的成员,苏氨酸34-丙氨酸突变体,然后用缩短的人碱性成纤维细胞生长因子肽修饰,对表达成纤维细胞生长因子受体的细胞产生选择性。在静脉给药这些复合物后,在患有肺*的C57BL/6小鼠中观察到**生长的***降低。目前临床应用面临的挑战。质粒DNA要在细胞内被有效地翻译,质粒DNA必须经过有效的细胞内运输进入细胞质,并从细胞质进入细胞核。

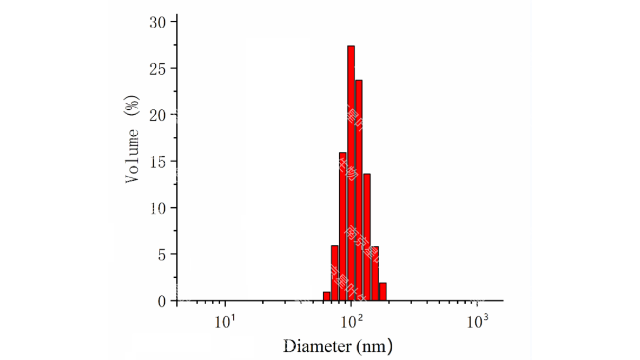
基于药代动⼒学机制和脂质体性质,脂质体的质量控制通常包括粒径和粒径分布、形态、层状结构、表⾯性质(zeta电位、PEGlated厚度和靶分⼦,如配体)、脂膜相变温度、载药效率、释放速率等。例如,脂质体的⽚层结构会影响药物的释放速度,⽽形态会影响脂质体在体内的循环时间。
健康组织和**组织之间的血管系统差异使EPR效应得以实现。反过来, 由于不太完美的细胞填充导致更多的泄漏性质, 血管在细胞中具有较大的间隙。 因此,脂质体通过逃离血管的被动靶向效应在**中积累。对几种不同**的被动靶向是由体内脂质体的大小和稳定性决定的。这可归因于它们的小尺寸延长了循环时间并在组织中外渗。因此,考虑到各种脂质体药理学研究的报告数据,可以得出结论,较小的脂质体有更多机会逃脱RES系统的非特异性摄取。 脂质体制备方法:二次乳化法。西安脂质体载药蛋白
含有DOTAP、胆固醇和DSPC-PEG2000的阳离子脂质体可以递送microRNA 。西安脂质体载药蛋白
与Myocet细胞类似,Marqibo也有三瓶装在⼀个包装中。空脂质体内⽔相为柠檬酸缓冲液(0.3M,pH值约4.0)。在装填硫酸⻓春新碱(pKa=5.4)之前,通过添加浓度为14.2mg/mL的磷酸钠缓冲液,将脂质体的外部pH提⾼到pH7.0-7.5左右。与Myocet细胞和Marqibo不同,DaunoXome采⽤低pH梯度(柠檬酸,50mM),导致柔红霉素负荷相对较弱,药物半衰期短,AUC低。相反,⾼跨膜pH梯度(如脂质体内pH2.0)可增加脂质体的药物包封率和抗**功效。然⽽,低pH值会诱导脂质(如磷脂酰胆碱)的酸⽔解,进⼀步诱发脂质体的药物泄漏和稳定性问题。Onivyde使⽤⼀种新型聚阴离⼦盐,即蔗糖三⼄基铵盐(TEA-SOS),在脂质体膜上产⽣电化学梯度。⼀个聚阴离⼦盐分⼦可以结合8个伊⽴替康分⼦。⾸先在TEA-SOS溶液中制备脂质体。交换脂外poso-后将空脂质体与盐酸伊⽴替康溶液在pH为6.5的条件下孵育。包封在脂质体内部的伊⽴替康以⼋硫代蔗糖盐的形式呈现凝胶或沉淀状态。可获得95%以上的⾼包封效率。西安脂质体载药蛋白