诱导式关节炎模型根据造模物质的不同进行分类,常见的有佐剂诱导型、胶原诱导型和胶原抗体诱导型关节炎。其中大鼠CIA模型的组织和免疫学改变与人RA**接近,AA模型的病情表现**为明显和持续。
(一)佐剂诱导型(AA)AA,又称为弗氏佐剂关节炎,介导溶剂分为完全佐剂(CFA)和不完全佐剂(IFA)。通常用CFA作介导剂,AA模型在T细胞相关致炎通路的药物筛选上发挥着重要的作用。
(二)胶原诱导型(CIA)CIA模型是由Trentham等于1977年***建立的实验性关节炎动物模型。通过皮下注射Ⅱ型胶原和等量CFA的混合液来建造,来源于鸡、小牛和大鼠的Ⅱ型胶原均能引起关节炎症。CIA是MHC相关型,以T/B淋巴细胞介导的关节炎症侵蚀为主要特征。
(三)胶原抗体诱导型(CAIA)抗Ⅱ型胶原单克隆抗体源自8周大的雄性DBA/1J小鼠CIA模型,这些抗体混合物注射到模型小鼠的关节腔后可直接作用于Ⅱ型胶原或其他在体内高表达的自身抗原,从而发挥免疫介导作用。该模型的临床症状与CIA和RA很相似,突出特点是能在几天之内迅速发病,关节组织中巨噬细胞和多核型白细胞浸润。该模型很好的体现了外源性抗原抗体刺激体诱导的严重关节损伤。 英瀚斯生物,可做实验动物模型行为学分析。福建构建实验动物模型怎么选择
精神分裂症实验动物模型,英瀚斯生物小编为您介绍。旷场行为测试主要用于衡量动物的自发活动性和探索新异事物的行为,二者分别用动物在旷场测试中的水平运动距离和直立次数来衡量。有研究表明,慢性MK-801给药(NMDA受体拮抗剂)能诱导大鼠自发活动性的改变,自发活动距离的增加或减少与给药剂量及测试时间有关。在社会隔离建立的拟精神分裂症动物模型中,隔离组大鼠表现出旷场自发活动性的明显的增加。旷场自发活动性的增加与精神分裂症的阳性症状密切相关。江苏承接实验动物模型实验实验动物模型的常见问题解答。
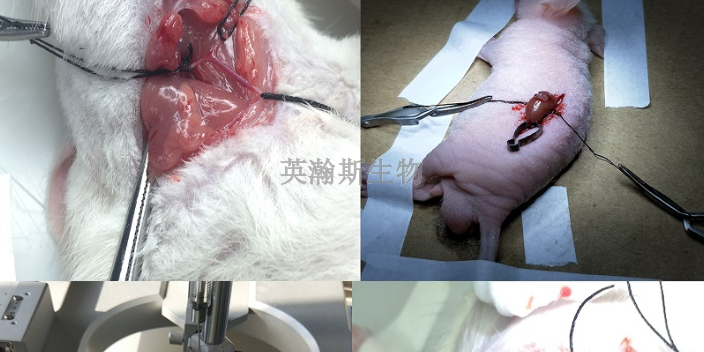
大鼠烫伤模型
(1)复制方法:按30mg/kg体重的剂量经腹腔注射3%戊巴比妥钠麻醉大鼠,根据体重腹部备皮,然后固定于实验台上。将大鼠移近加热自来水的烧杯,将纱布条浸入热水中,待水温恒定于99℃时,取出纱布,立即平铺于待烫部位,以纱布接触大鼠皮肤后计时。
(2)模型特点:大体观察:致伤3s大鼠局部皮肤发红、轻微水肿。愈合后毛发生长良好,有少量红褐色素沉着,皮肤轻微挛缩,表皮光滑。致伤10s大鼠局部皮肤发白、水肿。愈合后毛发生长良好,皮肤瘢痕形成,表面粗糙不平。光镜观察:致伤3s大鼠表皮层次尚清楚,细胞明显肿胀、变性,层次结构尚清楚,细胞核结构不清。表皮内有水疱形成,真皮水肿、间质疏松,胶原纤维断裂,嗜酸性染色性能减退,呈嗜双色性。致伤10s大鼠表皮细胞部分脱落,结构不清,明显变性、坏死,部分细胞已溶解。表皮内有水疱形成,真皮层间质疏松、充血,胶原纤维融合成片,嗜酸性染色性能减退,呈嗜双色性,大部分皮脂腺、汗腺、***被破坏,结构不清,真皮深部可见残余***。皮下组织血管扩张、充血、水肿明显,结构未破坏。上述结果表明,致伤3s大鼠为浅Ⅱ度烫伤,致伤10s大鼠为深Ⅱ度烫伤。
急性肺损伤与ARDS实验动物模型。急性肺损伤(ALI)是临床上较为常见的急危重症,是由心源性以外的各种肺内外致病因素导致的急性、进行性缺氧性呼吸衰竭。临床上以急性进行性加重的呼吸困难、呼吸窘迫、难治性低氧血症和非心源性肺水肿为早期表现,ALI严重阶段可发展为急性呼吸窘迫综合征(ARDS)。目前 ,ALI和ARDS是临床上急危重症医疗的重点、难点。而通过建立ALI和ARDS的动物模型是了解其主要发病机制及探索医疗方法的重要手段,人类研究中产生的假设可以在动物模型中进行测试,同时体外模型得到的实验结果也可以在动物模型中进行评价,也可应用于评估动物与人体疾病之间的联系。疾病实验动物模型制作,找英瀚斯生物。
5XFAD转基因实验动物模型。5XFAD小鼠在小鼠Thy1.2启动子的控制下过度表达人类APP和PSEN1蛋白,共有5个AD连锁突变,分别是APP中的瑞典(K670N/M671L)、佛罗里达(I716V)和伦敦(V717I)突变,以及PSEN1中的M146L和L286V突变。1.5个月大的5XFAD小鼠就开始出现Aβ沉积。5XFAD小鼠在大脑中积累的Aβ42多于Aβ40,这表明5个FAD突变累积影响Aβ42的产生。然而,在5XFAD小鼠中未观察到tau过度磷酸化和NFTs的形成。2个月大时出现星形胶质细胞增生和小胶质细胞增生,表明神经炎症发生在该模型早期。5XFAD小鼠再现了人类AD的病理学,类似于Tg2576、APP23和APPPS1模型。英瀚斯生物,可承接实验动物模型药效实验。吉林专业实验动物模型构建
英瀚斯生物,实验动物模型,饲养、造模、取材、检测一站式完成。福建构建实验动物模型怎么选择
新一代AD(阿尔兹海默症)实验动物模型。尽管APP-Tg小鼠在过去十几年中范围广的被用于开发新的AD医疗策略,但这种小鼠的基因表型和AD患者的还是不同。而且上述的转基因动物模型在Aβ的生成、tau蛋白的过度磷酸化、神经纤维缠结等病理特征上和AD患者的差异也很大,无法理想地模拟AD患者。为了克服这些不希望出现的问题,研究人员构建了带有Swedish(KM670/671NL)、Beyreuther/Iberian(I716F)和Arctic突变等APP基因敲入(APP-KI)小鼠。APP-KI小鼠在没有过度表达APP的情况下生成Aβ42。随着年龄的增长,APP-KI小鼠大脑皮层和海马区出现过多的Aβ沉积。另一方面,与其他AD模型一样,该模型没有tau病理、NFTs、神经退行性变或大量神经元丢失可用于研究临床前AD。由于基因组编辑的新的进展,尤其是CRISPR/Cas技术,未来对转基因动物模型进行改良也值得期待。福建构建实验动物模型怎么选择