外泌体的生成,微泡是由质膜的出芽形成的,膜双层通过磷脂的不对称分布来维持脂质的“多面性”。外层富含磷脂酰胆碱和鞘磷脂,而内层主要由磷脂酰丝氨酸和磷脂酰乙醇胺形成。然而,胞质Ca2+的内流可以破坏这种不对称性,导致磷脂跨膜双层的重新分配,促进膜起泡。依赖Ca2+的蛋白水解同时降解膜相关的细胞骨架,促进出芽过程。在外泌体形成过程中,首先,MVE(多囊体)向内芽形成小泡,内含来自细胞质的货物(蛋白质、mRNA和miRNAs)。然后,MVE要么与细胞膜融合释放外泌体(内囊泡),要么与溶酶体融合降解MVE含量。到达目的地后,外泌体通过内吞途径或与靶细胞膜融合,将其内容物释放到细胞质中。细胞的膜的囊泡也可以直接从细胞膜上萌发,携带活性蛋白、RNA和其他化合物。南京英瀚斯生物-外泌体检测服务_疾病医学模型_。浙江值得信赖的外泌体实验
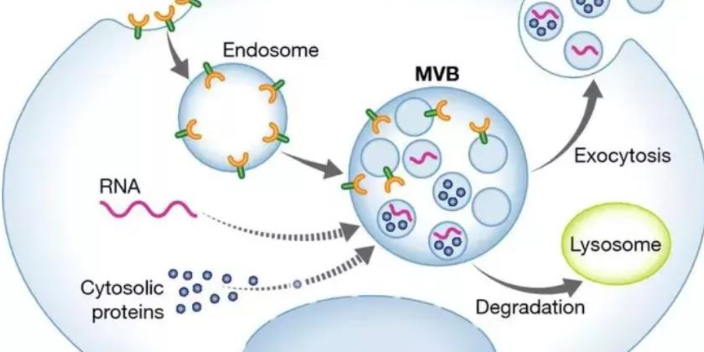
外泌体(exosome)*适用于通过特殊手段拿到的由胞内体来源的释放到细胞外的膜泡结构。建议对细胞外囊泡进行细分时使用物理上的界定如小细胞外囊泡(sEV)和中/大细胞外囊泡(m/lEV),或者高密度囊泡(high density)和低密度囊泡(low density)等,同时也建议使用表面蛋白来界定如CD63+CD81+细胞外囊泡等。当使用exosomes等称呼时应当进行严谨的实验证明使用的“exosomes样品”是由胞内体途径产生的。南京英瀚斯生物专业外泌体检测相关仪器齐全。安徽比较好的外泌体外泌体检测服务,经验丰富,操作熟练。
外泌体的提取主要包括以下几种方式。一是超速离心法,这是外泌体提取比较常用的方法。此种方法得到的外泌体量多,但是纯度不足,电镜鉴定时发现外泌体聚集成块,由于微泡和外泌体没有非常统一的鉴定标准,也有一些研究认为此种方法得到的是微泡不是外泌体。二是过滤离心,这种操作简单、省时,不影响外泌体的生物活性,但同样存在纯度不足的问题。三是密度梯度离心法,用此种方法分离到的外泌体纯度高,但是前期准备工作繁杂,耗时,量少。四是免疫磁珠法,这种方法可以保证外泌体形态的完整,特异性高、操作简单、不需要昂贵的仪器设备,但是非中性pH和非生理性盐浓度会影响外泌体生物活性,不便进行下一步的实验。五是PS亲和法,该方法将PS(磷脂酰丝氨酸)与磁珠结合,利用亲和原理捕获外泌体囊泡外的PS。该方法与免疫磁珠法相似,获得的外泌体形态完整,纯度比较高。由于不使用变性剂,不影响外泌体的生物活性,外泌体可用于细胞共培养和体内注射。2016.9《ScientificReports》杂志发表了该方法比较新数据,表明PS法可提取相当高纯度的外泌体
外泌分离后可以做蛋白,也可以做RNA(microRNA和LncRNA),36%的研究人员通过Westernblot或其他方法来鉴定蛋白,29%的人员利用qPCR对microRNA表达谱进行分析,9%利用芯片进行microRNA表达谱分析。同时,新一代测序的用户也不少,13%的人员利用NGS开展microRNA/小RNA研究,9% 开展mRNA研究。此外,目前的大部分工作还是停留在科研阶段,后续的生物标志物开发和验证不多,而诊断和疗法的开发就更少。Razvi认为,exosome的定性和定量研究是个快速发展的市场。同时,循环生物标志物的市场也存在着机遇和挑战。不过,无创产前检测技术的成功让人们相信,循环生物标志物有望在**及其他疾病的诊断上发挥作用。科研实验的外泌体检测服务介绍。
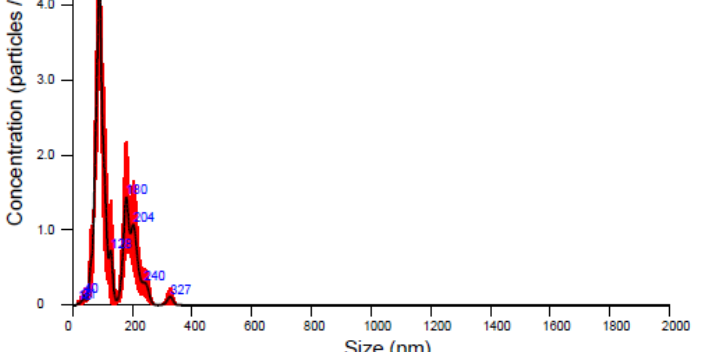
外泌体是一类由细胞分泌的病毒大小的膜状囊泡,它们携带有蛋白质与核酸,调节着胞内的沟通。目前较常用的外泌体提取方法是differential centrifugation (DC)——差速离心法。也有用试剂盒提取外泌体,但效率均不高。聚乙二醇(PEG)用于浓缩和纯化病毒已经超过50年,因为外泌体与病毒有着较为相似的生物物理特性,因此作者考虑用聚乙二醇来纯化外泌体,并且给出了新的浓缩提纯外泌体的方法。是一种直径约30~100nm的双层膜囊泡状结构小体,可由机体内多种细胞如免疫细胞、干细胞、心血管细胞、网织红细胞外泌体检测服务-价格低-周期短-数据清晰。海南专门做外泌体哪家好
外泌体检测服务 承接各类大医学实验!专业!可靠。浙江值得信赖的外泌体实验
外泌体和微囊泡的区别在于其生成的方式不同。从晚期内体来源产生的细胞外囊泡称为外泌体,从细胞膜直接出芽产生的细胞外囊泡称为微囊泡。二者的大小也有所不同,外泌体的粒子直径在40~100nm范围,微囊泡的粒子直径在100~1,000nm,但有报道发现也存在直径较小的微囊泡,所以无法明确从粒子大小来区分二者。外泌体是健康细胞和*细胞均可释放的小膜泡,***存在于人体的血液、乳汁、尿液以及唾液等多种体液中,其种类和数量与机体的生理状态息息相关。浙江值得信赖的外泌体实验