除了靶向成像,超声微泡造影剂还可用于提供***有效载荷。血管通透性的同时释放和增强,如下面更详细讨论的,是超声微泡技术所独有的属性。设计用于干预的微泡配方的一个关键组成部分是将***剂装载到外壳上。气体**本质上是一个不隔离有机化合物的空隙,而脂质外壳太薄(~3nm),无法容纳足够的货物。一种增强负载的方法是将油引入溶解亲水或亲脂药物的脂质壳中。这种形成声活性脂球(AALs)的技术在体外输送化疗药物方面取得了成功。当存在阳离子脂质或变性蛋白质时,带负电的***物质,如DNA或RNA,可以静电耦合到外壳上。该技术已***用于基因转染实验。实验中观察到的脂质包被微泡的负载能力约为0.01 pg/um'。超声已被证明可以增强溶栓,超声与微泡结合使用,在溶解血栓方面比单独使用造影剂或超声更成功。重庆超声微泡药物
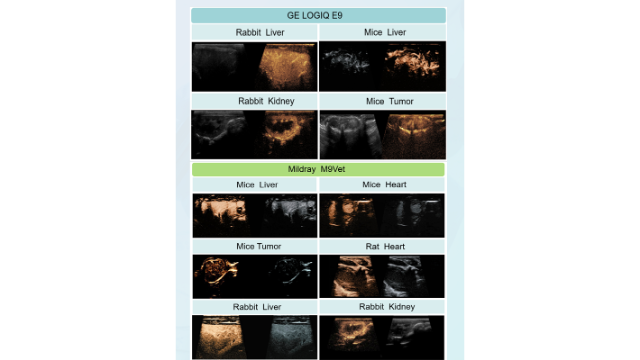
***个靶向微泡心脏成像研究是在急性缺血再灌注损伤模型中进行的,该模型在狗身上注射了涂有磷脂酰丝氨酸的白细胞靶向微泡,磷脂酰丝氨酸是颗粒吞噬摄取的标记物。这些微泡针对的是在血管中积累且尚未外渗的白细胞:在再灌注后1小时观察到**靶向的造影剂在梗死区积累。在心肌中观察到超声造影剂信号、中性粒细胞靶向放射性示踪剂的积累与髓过氧化物酶(炎症的酶标记物)之间的相关性。上述方法的对比机制是基于白细胞在缺血-再灌注损伤区与上调的细胞粘附分子(p-选择素、e-选择素、ICAM-1和VCAM-1)在血管内膜上的强烈结合现象。因此,不依赖白细胞作为微泡的二级捕获目标可能是更好的策略,而是设计真正的分子显像剂,直接结合内皮细胞上上调的p-选择素、e-选择素、ICAM-1或VCAM-1分子。这样的试剂已经可用,并在体外流动室设置以及模型体内系统中进行了测试。重庆超声微泡脂质载药超声微泡造影剂另一种选择是通过赋予超声微泡生物启发策略其中天然细胞膜可以用作构建超声微泡的材料。

***斑块的检测对于*******的发病率和死亡率可能更为重要。由于潜在的炎症,活性斑块区域的内皮细胞被***马托雷过程;因此,内皮细胞中这些位点上的VCAM-1和选择素应该被上调,用抗VCAM-1靶向微泡和抗p-选择素靶向或抗e -选择素靶向泡进行分子成像可能是有用的。在这种情况下,可用的动物模型是高胆固醇饮食的apoE⫺/⫺小鼠。**近,研究人员利用抗vcam -1抗体修饰的生物素化微泡成功靶向了这类小鼠主动脉弓内的斑块。由于大多数单克隆抗体本身可能无法在快速流动条件下靶向微泡,因此在同一链霉亲和素修饰的微泡上结合快速结合的生物素化SialylLewisx聚合物和紧密结合的生物素化抗vcam -1抗体可能会有所帮助。事实上,在高胆固醇饮食的apoE-/-小鼠中,这些配体组合的微泡靶向成功地在动脉血管区域积累,但在对照组小鼠中却没有,尽管有高剪切流量。
内皮素(CD105)是转化生长因子的受体,是一种增殖相关的低氧诱导蛋白,在血管生成内皮细胞上高度表达。使用99mTc-labeled单克隆抗体靶向内啡肽的免疫扫描显示,**中大量摄取内啡肽。**近,已经描述了一种将内啡肽特异性单克隆抗体偶联到微泡的新方法。通过超声将Avidin整合到微泡的外壳中,然后通过生物素与单克隆抗体结合。在体外证实了靶向内啡肽的配体定向微泡的积累。鉴于将多肽和单克隆抗体附着在微泡上的能力,人们可以设想靶向超声剂用于血管内皮生长因子(VEGF)、成纤维细胞生长因子(FGF)和金属蛋白酶组织抑制剂(TIMPS)的酪氨酸激酶受体的成像。如果这些气泡要在患者体内给药后与特定受体结合,就必须将靶向配体附着到微泡壳上。
**初的微泡靶向实验是在静态条件下进行的:将气泡与目标表面接触(通常是倒置),在没有流动的情况下孵育几分钟,然后将剩余的自由气泡洗掉,测量保留气泡的数量和声学响应。然而,这种情况并不是脉管系统内真正靶向的良好模型,在脉管系统内,结合发生时没有任何流动停止。取决于配体-受体结合和脱离动力学,以及配体和受体的表面密度、血流和壁剪切条件,与靶标的结合可能发生,也可能不发生。结合可能是短暂的(几分之一秒),也可能是长久的(几秒或几分钟),这取决于在初始接触期间有多少牢固的键有机会形成。了解微泡靶向性的比较好方法是在体外受控条件下,以已知的流速、配体和受体密度进行靶向性研究。平行板流室通常用于这些研究。一些配体(如抗体)能够与目标抗原牢固结合(一旦结合发生解离抗体和抗原可能需要几天的时间,但这种结合并不总是很快的。在流动的情况下,颗粒上的配体与受体结合的时间非常有限。在极端情况下(大血管中1米/秒的血流),典型的配体与受体结合位点线性尺寸为1纳米时,必须在1纳秒内发生有效结合,这是一个极短的时间,与大多数抗体-抗原kon动力学常数不相容。靶向超声造影剂的一个潜在应用是用于基因。供应超声微泡供应
这些配体组合的微泡靶向成功地在动脉血管区域积累,但在对照组小鼠中却没有,尽管有高剪切流量。重庆超声微泡药物
超声联合纳米微泡进行核酸输送超声联合纳米微泡进行DNA传递。不考虑超声穿孔现象,建议采用US与带核酸的微泡相互作用来提高传输效率。这种策略也可能有助于遗传物质的位点特异性释放,从而减少非共振组织转染。通过纳米微泡转移基因已经采用了几种技术,从基因的并发管理到纳米泡系统内的内涵。有多种方法,包括利用阳离子脂质组成纳米气泡的外壳用于DNA的静电附着,在制备过程中直接将DNA物理组装在外壳中,在外壳上应用阳离子聚合物层用于DNA的静电相互作用,携带DNA的纳米微泡载体的共价结合以及利用兼容的DNA链建立纳米微泡。分析发现,在体外,基于脂质的纳米微泡比基于白蛋白的纳米微泡引起几次基因转染。此外,在小鼠肝脏中也观察到脂基纳米微泡的主要基因转移。亚微米大小的气泡与传统的手持式超声检测仪器相结合,已被证明是一种高效的基因转移试剂。亚微米尺度的气泡被开发并建议作为一种有前景的基因传递方法。重庆超声微泡药物