- 品牌
- MCE,艾德莱,OriGene,abmart,ABW基质胶
未来,基质胶与类研究的结合将朝着更高的生物相容性和功能性发展。研究人员将致力于开发新型的生物材料,以更好地模拟体内微环境。此外,利用3D打印技术和生物工程手段,构建更复杂的类模型也将成为一个重要方向。这些新技术不仅可以提高类的结构和功能,还可以实现个性化医疗的目标。同时,基质胶的改良和优化也将与基因编辑技术相结合,为疾病模型的建立和药物筛选提供更精细的平台。总之,基质胶与类的研究将继续推动再生医学和个性化医疗的发展,为人类健康做出更大贡献。基质胶的透光性优化有利于类器官的长期活细胞成像。富阳区模基生物基质胶-类器官培养实验步骤
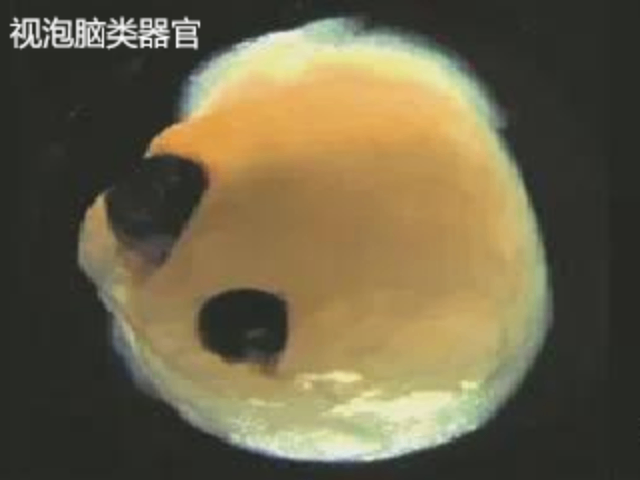
基质胶的制备和优化是类器官培养成功的基础。常见的基质胶制备方法包括从动物组织提取和合成生物材料。胶原蛋白基质胶是蕞常用的类型之一,其制备过程通常涉及将胶原蛋白溶液在特定条件下交联形成凝胶。为了提高基质胶的生物相容性和功能性,研究人员还可以通过添加生长因子、细胞外基质蛋白或其他生物活性分子来优化基质胶的成分。此外,基质胶的物理特性,如硬度、孔隙度和水合作用等,也可以通过调节成分浓度和交联条件来实现。通过这些优化措施,可以更好地满足不同类型类的培养需求。上城区高成功率基质胶-类器官培养供应商通过显微操作可精确控制基质胶中类器官的初始接种位置。

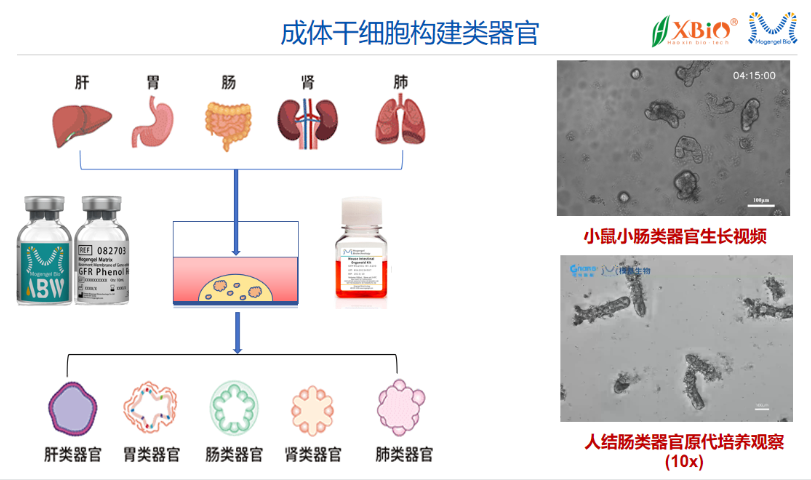
类***是由干细胞或组织特定细胞在体外培养形成的三维结构,能够模拟真实***的形态和功能。与传统的二维细胞培养相比,类***具有更接近生理状态的细胞排列和微环境,能够更好地反映***的生物学特性。类***的应用范围广泛,包括药物筛选、疾病模型建立和再生医学等领域。通过使用基质胶等支架材料,研究人员能够在体外重建复杂的组织结构,从而为新药研发和疾病机制研究提供更为真实的实验平台。此外,类***还可以用于个性化医疗,通过患者特异性细胞培养的类***进行药物敏感性测试,为临床***提供指导。
基质胶的生化组成直接影响类的发育方向和功能成熟度。天然基质胶(如Matrigel)虽然含有丰富的生长因子和ECM蛋白,但存在批次差异大的问题。为此,研究人员开发了多种优化策略:添加特定生长因子(如EGF、FGF等)来促进特定谱系分化;补充组织特异性ECM成分(如层粘连蛋白用于上皮类);或者使用重组蛋白构建成分明确的合成基质。的研究还关注基质胶中细胞因子的时空分布,通过构建生长因子梯度或开发刺激响应性释放系统,更好地模拟体内发育过程中的动态微环境。基质胶-类器官共培养技术可用于研究细胞微环境互作。
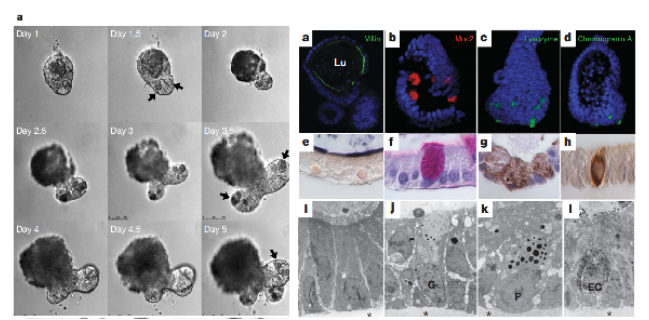
基质胶(如Matrigel或合成水凝胶)是类***培养的**支架,模拟体内细胞外基质(ECM)的物理和生化特性。其富含层粘连蛋白、胶原蛋白等成分,为干细胞或祖细胞提供黏附位点,并通过力学信号(如硬度、弹性)和生化信号(如生长因子)调控细胞行为。例如,肠类***培养中,基质胶的3D结构能促进隐窝-绒毛结构的自组织形成。优化基质胶的浓度(通常8-12mg/mL)和成分(如添加R-spondin1)可显著提高类***的存活率和功能成熟度。天然基质胶(如Matrigel)来源小鼠肉瘤,成分复杂但生物活性高,适合多数类***模型(如肝、胰腺)。但其批次差异性和动物源性可能影响实验可重复性。合成水凝胶(如PEG-based)可通过精确调控刚度、降解速率和功能化肽段(如RGD序列)实现定制化培养,适用于**类***或基因编辑研究。近期开发的脱细胞ECM(dECM)胶结合了两者优势,保留组织特异性信号的同时减少异源性风险,在心脏类***培养中已展现潜力。基质胶-类器官模型可用于研究胚胎发育过程中的形态发生。建德免疫共培养基质胶-类器官培养价格怎么样
基质胶的电纺丝改性可提高类器官培养的仿生性。富阳区模基生物基质胶-类器官培养实验步骤
尽管基质胶培养技术取得了明显进展,标准化仍然是面临的主要挑战。天然基质胶的批次差异、不同实验室的操作差异都会影响实验结果的可比性。为解决这些问题,需要建立统一的质控标准,包括基质胶的蛋白组成、生长因子含量、物理特性等关键参数的检测方法。自动化培养系统的开发可以减少人为操作差异,而标准化的类表征方法(如形态学分析、基因表达谱、功能测试等)则有助于结果的客观评估。此外,建立共享的类器官培养方案数据库将促进技术的规范化应用。富阳区模基生物基质胶-类器官培养实验步骤
- 上城区高成功率基质胶-类器官培养性价比高 2026-04-19
- 浙江基质胶-类器官培养批发厂家 2026-04-19
- 浙江高成功率基质胶-类器官培养如何申请试用 2026-04-18
- 湖州基质胶-类器官培养怎么用 2026-04-18
- 上城区肝癌基质胶-类器官培养怎么试用 2026-04-17
- 高浓度金牌低生长因子基质胶 2026-04-17
- 余杭区肿瘤基质胶-类器官培养性价比高 2026-04-17
- 宁波基质胶-类器官培养批发厂家 2026-04-17