- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
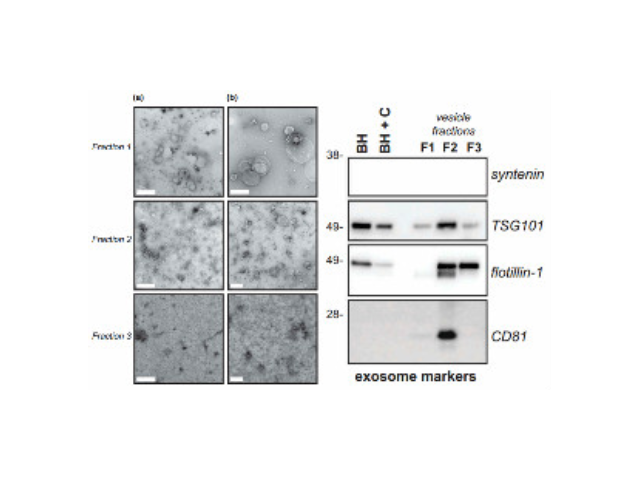
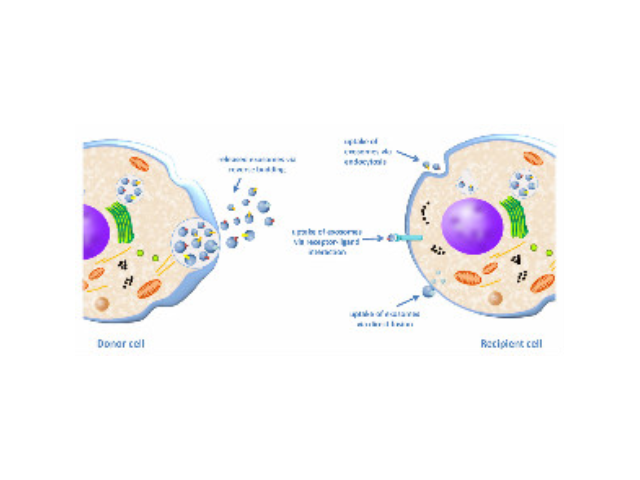
外泌体的形成与鉴定:首先,细胞膜内陷形成一个杯状结构,包括细胞表面蛋白和与细胞外环境相关的可溶性蛋白,导致早期胞内体(early-sortingendosome,ESE)的从头形成,或者是杯状结构直接和已经存在的ESEs融合;trans-高尔基体和内质网也能协助形成ESEs。ESE成熟后形成晚期胞内体(late-sortingendosomes,LSEs),较终形成MVBs(也称为多囊内小体)。MVBs是通过endosome限制膜向内凹(即质膜双凹)形成的,这一过程导致MVBs含有多个ILVs。MVB可以与溶酶体或自噬体融合,较终降解或与质膜融合释放作为外泌体的ILVs。外泌体表面蛋白包括四聚体蛋白、整合蛋白、免疫调节蛋白等。外泌体可以包含不同类型的细胞表面蛋白、细胞内蛋白、RNA、DNA、氨基酸和代谢物。使用可截留100KD分子量的膜,通过离心截留上清中的外泌体,截留完成后。外泌体的提取、分离方法:免疫亲和层析法。石家庄外泌体提取试剂厂家直销

外泌体与肺病预后:外泌体mirRNA和蛋白质被认为是NSCLC的预后因子。Dejima等在研究NSCLC患者预后的生物标志物时发现,外泌体miR-4257和miR-21的含量显着上升。此外,还有研究表明,低水平miR-146a-5p的NSCLC患者较高水平miR-146a-5p的NSCLC患者有更高的复发率。Sandfeld-Paulsen等在研究276例NSCLC患者血浆的外泌体时发现,NY-ESO-1是其中对低生存率有显着影响的标志物。Silva等利用TaqMan低密度芯片的方法系统分析了28位NSCLC患者体内的365种miRNA,其中let-7f、miR-30e-3p和miR-20b表达均下调,进一步研究发现,let-7f和miR-30e-3p水平可以区分早期和晚期NSCLC患者,高水平let-7f和miR-30e-3p与不良预后密切相关。如何高效地提取外泌体是实现这项新兴液体活检技术临床常规化应用的关键。武汉外泌体提取试剂产品介绍早先应用于从血清等样本中收集细菌,现在也被用来沉淀外泌体,其原理可能与竞争性结合游离水分子有关。

外泌体,是一种能被大多数细胞分泌的微小膜泡,具有脂质双层膜结构,直径大约40-100nm。尽管外泌体较初在1983年就被发现,但人们一直认为它只是一种细胞的废弃物。然而较近几年,人们发现这种微小膜泡中含有细胞特异的蛋白、脂质和核酸,能作为信号分子传递给其他细胞从而改变其他细胞的功能。这些发现点燃了人们对细胞分泌膜泡的兴趣。较近的研究发现外泌体在很多生理病理上起着重要的作用,如免疫中抗原呈递、一些病症的生长与迁移、组织损伤的修复等。不同细胞分泌的外泌体具有不用的组成成分和功能,可作为疾病诊断的生物标志物。
外泌体是一种存在于细胞外的多囊泡体,可通过细胞内吞泡膜向内凹陷形成多泡内涵体,内涵体与细胞膜融合后释放其中的小囊泡。外泌体的直径在40-110nm之间,其中包含RNA、蛋白质、microRNA、DN**段等多种物质,存在于血液、唾液、尿液、脑脊液和母乳等多种体液中。外泌体从发现至今已有30多年的历史,虽然较初被认为可能是细胞的“垃圾”,所以才被排出来,但是近年来研究表明外泌体具有功能活性并可进行细胞间信息传递。如今,研究已经发现外泌体在抗原提呈细胞中呈递抗原程中、一些病症细胞发生的发展、神经细胞信号转导过程中都发挥着重要作用。专利申请利用分离培养人尿液来源细胞并收集培养基来进行体外培养。现已证实可以分泌外泌体的细胞有:肥大细胞、淋巴细胞、树突状细胞、一些病症细胞、间充质干细胞等。
外泌体提取:1、过滤。超滤膜也可用于分离外泌体。根据外泌体的大小,从蛋白质和其他大分子中分离外泌体。较常见的过滤膜具有0.8μm、0.45μm或0.22μm的孔径,可用于收集大于800nm、400nm或200nm的外泌体,也有设计成微柱多孔硅纤毛结构以分离40-100nm外泌体:不过,该方法由于过滤膜的粘附,可能会损失外泌体,并且过滤时的压力和剪切力,可能会使外泌体变形受损。2、基于聚合物的沉淀技术。基于聚合物的沉淀技术通常包括将样本与含聚合物的沉淀溶液混合,在4℃温育并低速离心。用于聚合物沉淀的较常见聚合物之一是聚乙二醇(PEG)。用这种聚合物沉淀具有许多优点,包括对分离的外泌体影响小、pH中性等。目前大多数快速分离外泌体的商品化试剂盒都是基于此方法。然而基于聚合物的沉淀方法可能会同时分离非囊泡污染物(包括脂蛋白)而且,聚合物材料的混杂可能会影响下游分析。外泌体提取:较常见的过滤膜具有0.8μm、0.45μm或0.22μm的孔径。郑州正规外泌体提取试剂直销厂家
用无菌针管吸取上层含有外泌体的液体,置于80℃储存备用。石家庄外泌体提取试剂厂家直销
外泌体(exosome)是所有细胞释放出的菌类大小的颗粒。它们天然地存在于血液中。根据来自美国德州大学MD安德森一些疾病中心的一项新的研究,对外泌体进行基因操纵可能提供一种新的胰腺病治病方法。论文通信作者为德州大学MD安德森一些疾病中心一些疾病生物学系研究员RaghuKalluri博士。在这项新的研究中,经过基因修饰的外泌体(被称作iExosome)能够运送特异性地靶向KRAS突变基因的小RNA分子,从而导致胰腺病模式小鼠病情缓解,增加它们的总存活率。这些研究人员采用了一种被称作RNA干扰(RNAi)的靶向方法:利用这些天然的纳米颗粒(即外泌体)运送小干扰RNA(siRNA)或短发夹RNA(shRNA)分子来靶向胰腺病细胞中的KRAS突变基因,从而影响多种胰腺病模型的一些病症负荷和存活。他们证实外泌体能够作为一种高效的RNAi载体发挥作用,这是因为这些纳米大小的囊泡(即外泌体)轻松地在体内迁移和进入靶细胞(包括病细胞)中。外泌体在免疫中抗原呈递、一些病症的生长与迁移、组织损伤的修复等生理病理上起着重要的作用。石家庄外泌体提取试剂厂家直销
外泌体提取:尺寸排阻色谱。尺寸排阻色谱(Size-exclusionchromatography,SEC)是基于大小而非分子量实现分离大分子。该技术应用填充多孔聚合物微球的柱子,分子根据其直径通过微球,半径小的分子需要更长的时间才能通过色谱柱的孔隙迁移,而大分子则从色谱柱中更早地洗脱。尺寸排阻色谱可以精确分离大小分子。此外,可以将不同的洗脱溶液应用于该方法。与离心方法相比,色谱分离已被证明具有更多优势,因为通过色谱分离的外泌体不受剪切力的影响,这可能会改变囊泡的结构。目前,SEC是一种普遍接受的分离血液和尿液中外泌体的技术。不过,该方法耗时较长,不适合大量样本处理。外泌体的提取、分离方法:超高...
- 昆明正规外泌体提取试剂产品介绍 2026-05-23
- 武汉正规外泌体提取试剂哪里买 2026-05-23
- 成都外泌体提取试剂厂家 2026-05-23
- 重庆正规外泌体提取试剂供应商 2026-05-23
- 合肥外泌体提取试剂哪里买 2026-05-23
- 北京外泌体提取试剂厂家供应 2026-05-23
- 昆明正规外泌体提取试剂平均价格 2026-05-23
- 杭州正规外泌体提取试剂直销厂家 2026-05-23
- 正规外泌体提取试剂哪家便宜 2026-05-23
- 厦门正规外泌体提取试剂生产厂家 2026-05-23
- 太原外泌体提取试剂直销价 2026-05-22
- 贵阳正规外泌体提取试剂厂家供应 2026-05-22
- 郑州正规外泌体提取试剂厂家推荐 2026-05-19
- 天津外泌体提取试剂直销厂家 2026-05-19
- 郑州正规外泌体提取试剂销售厂家 2026-05-19
- 外泌体提取试剂平均价格 2026-05-19


- 安徽品质好的糖原染色试剂盒哪家便宜 05-24
- 济南RNA提取试剂服务电话 05-23
- 开封无血清细胞冻存液平均价格 05-23
- 安徽哪家提供糖原染色试剂盒厂家批发价 05-23
- 福建咨询糖原染色试剂盒生产厂家 05-23
- 深圳正规鼠尾胶原报价 05-23
- 无锡广州细胞外基质胶 05-23
- 昆明正规外泌体提取试剂产品介绍 05-23
- 厦门正规RNA提取试剂销售厂家 05-23
- 太原细胞高效转染试剂厂家批发价 05-23