医疗器械设计开发的难点之一是满足严格的合规性标准。医疗行业的产品受到一系列法规和标准的监管,例如ISO 13485和FDA的规定。设计团队必须牢记这些法规的要求,并确保设计过程中的每一步都符合相关标准,以保障产品的质量和合法上市。 临床前研发是医疗器械设计开发过程中的一个决定性阶段。在这个阶段,团队通过实验室测试、仿真模拟和小规模实际应用,验证产品的性能、安全性和有效性。通过不断地改进和优化,团队能够确保产品在进入正式临床试验前已经达到高水平的可行性和可靠性。 CDMO通过提供一体化的服务,加速了医疗器械从概念到市场的转化过程。医疗器械设计

设计验证和确认是确保产品符合质量和合规标准的重要步骤。CDMO服务商通过建立成熟的项目管理体系,可以在这些关键步骤中提供支持。他们在设计验证时会使用各种工具和技术,确保产品的性能和可靠性达到预期。 在医疗器械设计开发的早期阶段,企业可能面临资源配置不足的问题。CDMO服务商可以为企业提供弹性的资源配置,根据项目需求灵活调整团队规模,确保项目能够按时按质完成。 CDMO服务商通常拥有先进的制造技术和设备,能够为医疗器械产品提供高质量的原型制作和批量生产。他们熟悉医疗器械行业的相关法规和标准,确保产品的生产过程符合质量管理要求。医疗设备外观设计专业的设计开发团队对医疗器械企业的成功至关重要。
设计开发过程中的风险管理至关重要。思脉得拥有专业的风险评估团队,能够及早识别和处理潜在的风险因素,降低项目风险。 医疗器械的材料选择对产品的安全性和可靠性至关重要。思脉得在材料科学和工程方面有着丰富的经验,能够为客户提供适用的材料解决方案。 思脉得医疗科技集团的项目管理体系结合客户需求,提供高效的设计开发方案。我们的项目管理团队协同工作,确保项目按时交付、在预算内完成。 医疗器械设计需要在合规性和创新性之间找到平衡点。思脉得的设计开发团队在此方面有着丰富的经验,能够在法规要求的基础上为产品增添创新元素。
在ISO13485文件中明确了医疗器械设计开发的一系列要求,主要从设计和开发策划、设计和开发输入、设计和开发输出、设计和开发评审、设计和开发验证、设计和开发确认、设计和开发转换、设计和开发更改的控制、设计和开发文件几方面进行了描述。思脉得医疗科技集团秉承创新技术和服务,为客户提供超预期价值为宗旨,致力于为医疗行业客户提供全套技术解决方案,为不同客户提供定制化的设计开发服务,涵盖产品需求分析、项目计划、概念设计、详细设计、样品制作、设计验证、产品注册等。如果您有相关需求,请与我们联系。CDMO的发展助推了医疗器械行业向更高水平发展。
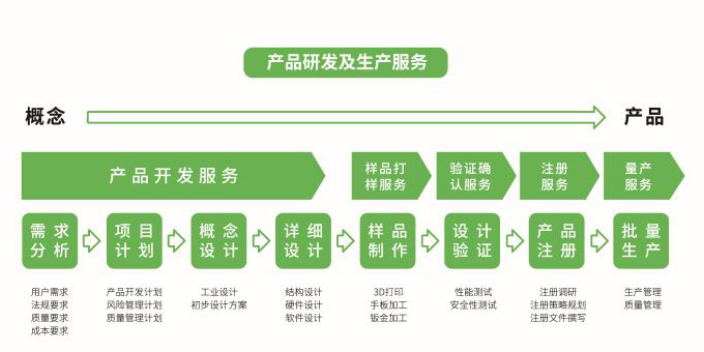
思脉得医疗科技集团拥有一支行业经验丰富的设计开发团队,依托于丰厚的企业资源,已经建立了一套成熟的项目管理体系,可以结合客户需求,从客户需求、法规要求、质量要求、成本要求多方面考量,提供定制化的设计开发方案,高效、高质量的实现委托企业的开发需求。不仅避免了资源的浪费,还将促进行业资源配置优化,并且助力企业一起将研究成果转化为具有市场销售潜力与竞争力的医疗器械产品。思脉得医疗科技集团秉承创新技术与服务,为客户提供超预期价值为宗旨,致力于为医疗行业客户提供全套技术解决方案。CDMO(医疗器械外包制造服务)在医疗行业中扮演着越来越关键的角色。深圳医疗设计
CDMO通过专业的外包服务,帮助企业优化资源配置,降低开发风险。医疗器械设计
思脉得医疗科技集团的专业设计开发团队可以提供技术解决方案。团队通过与客户密切合作,确保产品的设计满足市场需求和法规要求。 选择合适的材料是医疗器械设计中至关重要的决策之一。思脉得在材料科学和工程方面有着深厚的经验,能够为客户提供适用的材料解决方案。 企业可以将设计开发外包给专业服务商,减少资源浪费,提高效率。思脉得医疗科技集团通过提供设计开发服务,帮助客户降低风险,提高项目成功率。思脉得医疗科技集团在设计开发过程中的风险管理方面拥有丰富的经验。我们通过系统的风险评估,及时发现和处理潜在风险,确保项目的顺利进行。 设计阶段的合规性考量是确保医疗器械上市的前提。思脉得在设计团队的指导下,以法规和标准为依据,确保产品的合规性,为上市做好充分准备。 思脉得医疗科技集团的专业设计开发团队可以为医疗器械企业提供技术支持。我们以创新和质量为重心,帮助客户在竞争激烈的市场中脱颖而出。医疗器械设计