当前,医疗器械行业的设计开发输入质量参差不齐。加强法规对设计开发输入的要求,提高行业对设计开发输入的重视程度,提高产品性能评价和质量管理体系的应用质量水平,可以更好地满足高标准高要求医疗器械行业的高质量发展。委托一家专业的第三方技术服务公司,不仅可以优化企业内部的资源优化,同时也响应了注册人制度下专人做专事的政策要求。思脉得医疗科技集团秉承创新技术和服务,为客户提供超预期价值为宗旨,致力于为医疗行业客户提供全套技术解决方案,为不同客户提供定制型的设计开发服务,具体涵盖产品需求分析、项目计划、概念设计、详细设计、样品制作、设计验证、产品注册等。如果您有相关需求,请与我们联系。思脉得医疗科技集团在注册人制度的支持下,提供临床前研发外包服务。全套医疗器械设计开发介绍
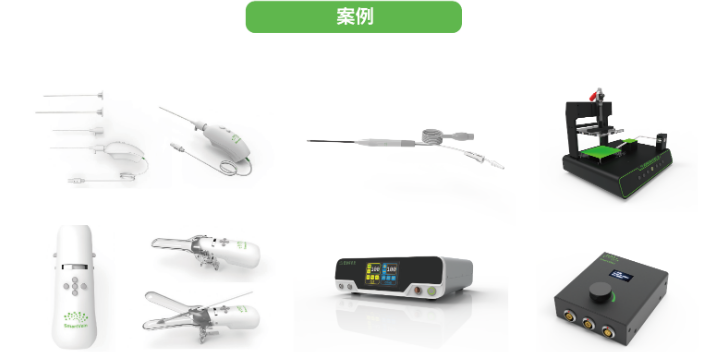
医疗器械的注塑技术应用广,尤其在生产小型零部件方面更为明显。通过合理设计模具结构和选择合适的材料,注塑技术不仅提高了生产效率,还降低了成本,为医疗器械制造注入了新的活力。 设计验证的过程旨在确保产品设计的可行性和合规性。通过严格的实验室测试和仿真验证,设计团队能够发现潜在问题并及时加以解决,确保产品的设计方案是可靠的。 CDMO服务商不仅在技术方面提供支持,同时在生产流程的优化上也有独到之处。他们拥有先进的生产设备和经验丰富的团队,可以提高生产效率,保障产品质量。医疗器械产品设计与开发CDMO服务模式可以使医疗器械企业更加灵活应对市场变化。

CDMO服务作为医疗器械行业的一个重要支柱,为企业提供了外包设计开发和生产制造的选择。企业可以将研发风险分担给专业的CDMO服务商,从而更专注于业务。思脉得医疗科技集团作为一家多元化服务商,通过其完善的CDMO服务,实现了设计到生产的全过程管理,满足了客户对高质量医疗器械的需求。 ISO 13485等医疗器械质量管理标准的严格遵守对于设计开发过程至关重要。思脉得在其项目管理体系中整合了这些标准,以确保产品符合法规要求。合规性不仅是法定要求,也是确保产品质量和安全性的必要条件。
《医疗器械监督管理条例》中明确指出,医疗器械监管的主要目的之一就是保证医疗器械的安全有效。《医疗器械注册备案管理办法》第三条规定,医疗器械注册是对提交注册的医疗器械的安全性、有效性和质量可控性进行审查,并决定是否批准申请的过程。设计是实现产品安全性和有效性的重要环节之一。在医疗器械产品的整个生命周期中,设计和开发是产品质量的基础,产品注册信息是设计和开发活动成果的一部分。设计和开发的输入基本上可以视为设计和开发过程中极其重要的环节,是后续设计和开发活动的基础,是识别和定义需求的过程,对注册申请资料的符合性有重要影响。注册人制度的实施推动了医疗器械企业对CDMO服务的需求增长。

专业团队的经验丰富 思脉得医疗科技集团拥有一支经验丰富的设计开发团队。这个团队不仅具备医疗领域的专业知识,还在多个项目中积累了丰富的实战经验。通过长期的实践,团队不断总结经验,形成了一套成熟的项目管理体系,能够高效、高质量地完成设计开发任务。 全产业链服务的管理优势 思脉得医疗科技集团的设计开发流程涵盖了从产品需求规范到上市准备的全产业链服务。这种全产业链服务的管理优势体现在项目管理的协同性上。团队能够更好地整合各个环节,确保每个阶段都得到精细管理,从而提高整体项目的执行效率。CDMO服务商的全产业链支持可以帮助企业快速响应市场需求。医疗器械设计网站
CDMO通过专业的外包服务,帮助企业优化资源配置,降低开发风险。全套医疗器械设计开发介绍
2019年4月,国家药品监督管理局印发《关于实施中国药品监管科学行动计划的通知》,围绕“创新、质量、效率、体系、能力”主题,推动监管理念创新,开展药品监管科学研究。针对新时期药品、医疗器械和化妆品监管存在的突出问题,通过创新监管工具、标准和方法,进一步增强监管工作的科学性、前瞻性和适应性,更好满足新时代公众对药品的需求。对安全的新需求。设计和开发输入是研发过程的重要组成部分。针对其在法规和质量管理体系方面的要求,加强对行业现状和监管新方法的研究,进一步明确要求,切实加大投入力度,提高设计开发输入的合规性、一致性。全套医疗器械设计开发介绍