肺纤维化模型不仅模拟了肺纤维化的病理过程,更深入地揭示了疾病发展过程中细胞间相互作用的变化。在这个模型中,多种细胞类型如上皮细胞、成纤维细胞、免疫细胞等共同参与,并形成了复杂的细胞网络。随着疾病的进展,这些细胞间的相互作用会发生明显变化。例如,上皮细胞受损后可能释放炎症介质,刺激成纤维细胞增殖并产生过多的胶原蛋白,形成纤维组织。同时,免疫细胞的激发和迁移也会影响炎症反应的强度和持续时间。这些细胞间相互作用的变化不仅推动了肺纤维化的进展,也影响了疾病的临床表现和疗愈效果。因此,通过肺纤维化模型,研究人员可以更普遍地了解细胞间相互作用的机制,为疾病的疗愈提供新的思路和方法。肺纤维化模型可以模拟不同类型的肺纤维化,如特发性肺纤维化。吉林比较好的肺纤维化模型造模方法
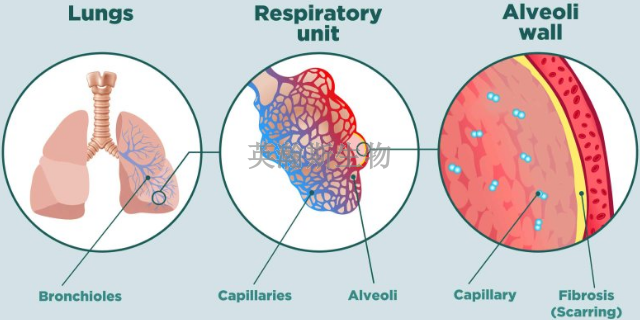
肺纤维化形成***组织。***一旦形成,便是长久性的。基于疾病的不同,可采取如下方式延缓疾病进展,开展预防:特发性肺纤维化的疗愈选择非常有限。尽管研究试验仍在进行,目前为止没有证据表明任何药物可以明显改善病情。重症病例单独可能的疗愈选择是肺移植。某些类型的肺纤维化对皮质类固醇(如泼尼松)及其他免疫抑制药物产生反应,因此有时会使用这些药物减缓纤维化过程。免疫系统在多种肺纤维化的发展中发挥着中心作用。使用免疫抑制剂(如皮质类固醇)的目的是减少肺部炎症和伴随的瘢痕形成。病情对药物疗愈的反应不尽相同。免疫抑制疗愈有效的患者或许并非患有特发性肺纤维化,特发性肺纤维化尚无明确的疗愈方法。吉林比较好的肺纤维化模型造模方法在肺纤维化模型中,肺泡壁会逐渐增厚,导致肺功能下降。
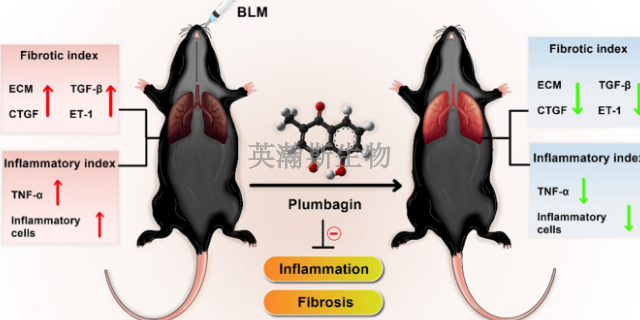
肺纤维化模型的并发症可能包括:肺部***(肺高压)。不同于全身性***,这种疾病只会影响肺部动脉。当瘢痕组织挤压比较细小的动脉和***时,会增加肺部血流阻力,从而导致这种疾病。这转而增加了肺动脉和右下心腔(右心室)内的压力。某些类型的肺高压是严重疾病,会逐渐恶化,有时甚至会致命。右心衰竭(肺源性心脏病)。当心脏右下心腔(心室)必须比平时更用力地泵送血液才能通过部分阻塞的肺动脉时,就会发生这种严重疾病。呼吸衰竭。这往往是慢性肺病的***阶段。当血氧水平下降至危险低水平时就会发生这种情况。肺*。长期肺纤维化也会增加您患肺*的风险。肺部并发症。随着肺纤维化恶化,可能会导致肺部血凝块、肺萎陷或肺部***等并发症。
为了更好地模拟IPF的复杂发病机制,特别是其中涉及的遗传易感性和肺泡上皮细胞功能障碍,研究人员开发了一系列遗传性肺纤维化模型。这些模型通常涉及对与IPF相关的关键基因进行敲除或突变。例如,马兰戈尼综合征(Marangoni syndrome)相关的表面活性物质蛋白 $\text{C}$(SP-C)突变小鼠模型,这些突变会导致肺泡上皮细胞凋亡和应激反应,**终自发性发展出肺纤维化。另一个重要的遗传学模型是端粒酶逆转录酶(TERT)缺陷小鼠模型,该模型模拟了人类中与端粒缩短相关的家族性肺纤维化,展示了上皮细胞衰老和功能障碍在疾病发病中的关键作用。这些遗传模型比较大的优势在于它们能在没有外部急性损伤的情况下,通过内源性机制逐渐发展出纤维化,从而更真实地模拟人类IPF的隐匿性、慢性进展性特征,是研究疾病早期驱动因素和遗传易感性的理想平台。肺纤维化模型为研究肺纤维化的环境因素提供了便利。
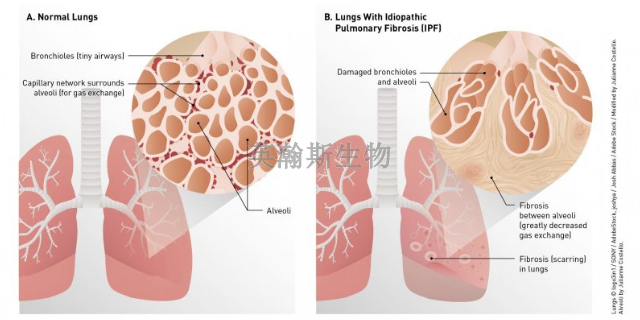
在肺纤维化模型中,一个明显且关键的变化就是肺泡壁的逐渐增厚。这个过程是由于持续的炎症、细胞损伤和修复机制的异常活跃所导致的。随着炎症的持续存在,免疫细胞会不断释放炎症介质,这些介质会刺激肺泡壁中的细胞增殖,并导致胶原蛋白和其他纤维组织的过量沉积。随着时间的推移,这些沉积物不断积累,使得肺泡壁变得坚硬而厚实,从而限制了肺泡的扩张和收缩能力。这种增厚不仅影响了气体的交换效率,还使得肺部难以有效地进行氧气和二氧化碳的交换,比较终导致肺功能的明显下降。这一过程在肺纤维化模型中得到了精细的模拟,为研究疾病的进程和疗愈提供了重要的参考。研究人员通过肺纤维化模型发现了一些新的疾病标志物。福建专业的肺纤维化模型造模方法
在肺纤维化模型中,上皮细胞的损伤和修复对肺纤维化的进程有重要影响。吉林比较好的肺纤维化模型造模方法
关于肺纤维化模型,目前肺纤维化的发展机制尚未完全明确,缺乏有效的疗愈方法来应对肺纤维化成为了一个现实问题。因此,一个理想的肺纤维化模型,不仅有助于进一步筛选肺纤维化生物标志物,同时也能为深入研究肺纤维化发病机制及动物临床疗愈肺纤维化和研发新药提供科学基础。其中,小鼠与大鼠因其体型小、价格便宜、操作简便等优点,成为目前肺纤维化动物模型构造中的比较普遍的选择。英瀚斯生物专业进行大鼠肺纤维化模型和小鼠肺纤维化模型的构建。吉林比较好的肺纤维化模型造模方法