- 品牌
- 同顺生物
诺拉曲特(Nolatrexed,CAS号147149-76-6)不仅在医治肝疾病方面展现出广阔前景,其在其他疾病医治领域的研究也在不断深入。目前,诺拉曲特用于医治结肠直肠疾病、肺疾病、前列腺疾病、胰腺疾病和头颈部疾病的研究已在美国、英国、加拿大、意大利和南非等国进入Ⅱ期试验阶段。作为胸苷酸合成酶抑制剂,诺拉曲特通过精确作用于疾病细胞内的关键酶,实现对疾病生长的有效控制。其独特的药物结构使其能够在胸苷酸合成酶中占有较大空间,并与酶的两个叶酸位置结合,从而高效抑制酶的活性。这种作用机制不仅增强了药物的抗疾病效果,还降低了对正常细胞的损伤。诺拉曲特在溶解度、储存稳定性和溶液配制等方面也表现出良好的特性,为其在临床上的普遍应用提供了有力支持。随着研究的不断深入,诺拉曲特有望为更多疾病患者带来新的医治选择和希望。原料药生产过程中产生的废弃物需合规处理,避免环境污染。美法仑生产
在特殊人群应用中,地拉罗司展现了良好的安全性与适应性。针对2岁以上儿童患者,分散片剂型可溶于果汁或水服用,提高依从性。Ⅲ期临床试验显示,儿童组不良事件发生率与成人相当(32% vs 35%),但3级以上不良反应(如胃肠道出血)发生率更低(4% vs 7%)。对于非输血依赖性地中海贫血(NTDT)患者,地拉罗司可有效控制铁过载,使血清铁蛋白水平平均下降412μg/L。在老年患者中,虽需警惕基础疾病对药物代谢的影响,但剂量调整至20mg/kg/d时,仍能维持85%以上的铁排除效率。长期毒性研究提示,连续用药5年未发现严重部位损伤,只见轻度可逆性晶状体浑浊(发生率12%)。值得注意的是,地拉罗司在妊娠期属于C类用药,动物实验显示高剂量(75mg/kg/d)可能致胚胎发育迟缓,但临床尚未见明确致畸报道。这些特性使其成为覆盖全年龄段、多类型铁过载疾病的稳定医治选择。美法仑生产原料药的仿制药生产需通过一致性评价,确保疗效一致。
该药物的药代动力学特性凸显了其临床应用的便捷性。口服后1.5-4小时达血药浓度峰值,生物利用度受食物影响较小,但高脂饮食可使峰浓度提升35%。其代谢主要依赖肝脏UGT1A1酶,半衰期为8-16小时,支持每日单次给药的方案。值得注意的是,地拉罗司是CYP3A4强诱导剂,同时抑制CYP2C8和CYP1A2酶活性,这种双重作用可能导致联用药物的血药浓度波动。例如,与华法林合用时需监测INR值,因CYP2C8抑制可能使华法林代谢减慢。在药物相互作用研究中,地拉罗司使辛伐他汀AUC增加2.3倍,提示需调整联用剂量。其排泄途径以粪便为主(80%),肾脏排泄只占8%,这种特性对肾功能不全患者具有安全优势。临床数据显示,在肌酐去除率>30 mL/min的患者中,无需调整剂量即可维持稳定疗效。
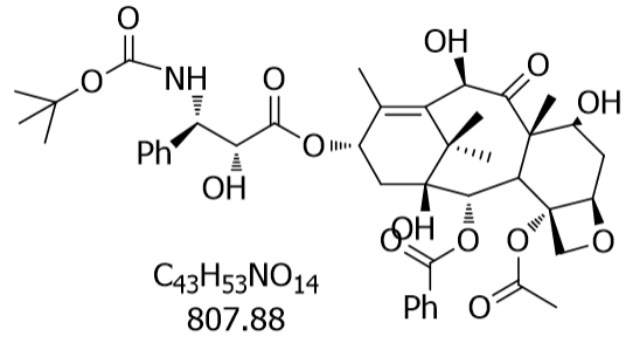
安全性管理是多西他赛临床应用的重要挑战。骨髓抑制作为常见不良反应,3-4级中性粒细胞减少发生率达75%-90%,但通过G-CSF支持可使发热性中性粒细胞减少发生率从29%降至6%。过敏反应呈现双相特征:早期反应(用药后10分钟内)以脸红、皮疹为主,发生率约10%;晚期反应(用药后1-3小时)可出现低血压、支气管痉挛,发生率约3%。预处理方案(8mg bid连用3天)可使严重过敏反应发生率从27%降至2%。体液潴留综合征在用药4周期后累积发生率达60%,表现为外周水肿(45%)、胸腔积液(12%)和腹水(8%),联合皮质类固醇预处理可使发生率降低至25%。神经毒性方面,2%患者出现3级感觉神经病变,表现为手套袜套样分布的麻木、刺痛,停药后3个月内可完全恢复。心脏毒性虽发生率低(<2%),但需警惕与蒽环类药物联用时的叠加效应,左室射血分数下降>15%时应暂停用药。特殊不良反应包括指甲改变(色素沉着、脱落发生率约15%)和眼毒性(结膜炎发生率8%),建议用药期间避免冷刺激以减少神经毒性加重风险。流化床制粒技术使原料药颗粒均匀度CV值≤8%,休止角≤35°。
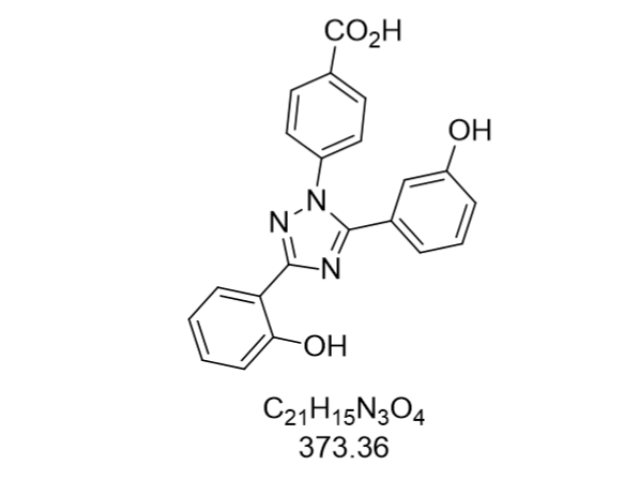
当前,诺拉曲特的研发正处于关键转折点。Eximias制药在2025年公布的肝疾病Ⅲ期研究中期分析显示,试验组与对照组的中位生存期分别为10.2个月和7.5个月(HR=0.78,95%CI:0.62-0.98),达到统计学明显性差异。中国作为肝疾病高发区,贡献了超过40%的入组病例,其结果将直接影响药物在中国NMPA的审批。与此同时,针对耐药机制的研究取得突破,发现TS酶T313I突变可导致药物结合力下降80%,而联合PARP抑制剂可逆转这种耐药。在适应症拓展方面,胰腺疾病Ⅱ期试验显示,与吉西他滨联用可使中位生存期延长至9.1个月,较单药的方案提升37%。随着2026年全球上市申请的推进,诺拉曲特有望成为基于结构生物学设计的TS抑制剂类抗疾病药,其研发路径也为同类药物开发提供了从靶点验证到临床转化的完整范式。原料药的多晶型现象影响药物性能。吉林原料药
多肽类原料药市场增速达15%,GLP-1受体激动剂需求激增是主因。美法仑生产
在临床开发进程中,已完成多项I/II期试验,验证了其安全性和初步疗效。2011年启动的NCT01348919试验针对复发/难治性MM患者,采用口服给药(10 mg/kg,每周两次),结果显示客观缓解率(ORR)达42%,中位无进展生存期(PFS)为5.8个月,且3级以上不良反应发生率较静脉注射制剂降低37%。另一项NCT01023880研究则探索了德兰佐米与硼替佐米的序贯医治模式,发现先使用德兰佐米可明显降低后续硼替佐米医治时的周围神经病变发生率(从28%降至12%)。药代动力学数据显示,该药物口服生物利用度达62%,半衰期为9.2小时,支持每日两次的给药的方案。值得注意的是,在老年患者(≥65岁)亚组分析中,单药医治的被染发生率较对照组降低19%,这与其对免疫细胞的保护作用密切相关。美法仑生产
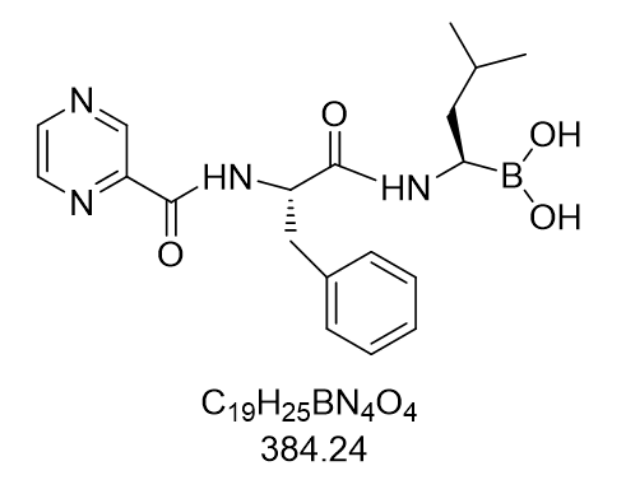
从市场格局到医治范式,硼替佐米的影响力已超越单一药物范畴。自2005年在中国获批上市(商品名万珂®)以来,其销售额从2010年的1.2亿元增长至2020年的5.39亿元,尽管2021年纳入第四批国家集采后价格下降65%,但销量增长使市场份额仍保持稳定。目前,国内企业通过一致性评价,形成原研+4家国产的竞争格局。在临床实践中,硼替佐米已从单药医治向联合方案演进:与免疫调节剂(来那度胺)、CD38单抗(达雷木单抗)、组蛋白去乙酰化酶抑制剂(帕比司他)的联用,使MM患者的微小残留病灶(MRD)阴性率从45%提升至72%。原料药质量标准会随技术发展更新,企业需及时跟进调整。四川多西他赛 Docetax...
- 吉林沙库比曲缬沙坦钠 2026-04-02
- 福建紫杉醇 2026-04-01
- 地拉罗司生产商 2026-04-01
- 沙库比曲缬沙坦钠供应公司 2026-03-31
- 兰州美法仑 2026-03-30
- 苯丁酸氮芥多少钱 2026-03-30
- 河北苯丁酸氮芥 2026-03-30
- 卡巴他赛价位 2026-03-28
- 无锡原料药 2026-03-28
- 宁夏德兰佐米 2026-03-28


- 常州7-氟-2-吲哚酮 04-24
- 宁波3-氨基-4-甲基苯甲酸乙酯Ethyl 3-Amino-4-methylbenzoate 04-24
- 4-(4-(4-甲基哌嗪-1-基)哌啶-1-基)苯胺生产厂 04-24
- 嘉兴紫杉醇侧链中间体(3R 04-24
- 紫杉醇侧链酸(五元环)厂商 04-24
- 合肥(4-溴苯)乙胺 04-24
- 苯磺酰胺Benzenesulfonamide生产商 04-24
- 陕西3-苯并呋喃酮 04-24
- 河北2-苄氧基乙醇 04-23
- 北京3 04-23