肺纤维化模型在研究肺纤维化与其他肺部疾病关系方面发挥了重要的作用,为科学家们提供了宝贵的实验平台。肺纤维化并非孤立存在,它常常与其他肺部疾病如慢性阻塞性肺疾病(COPD)、间质性肺病等交织在一起,相互影响。通过肺纤维化模型,研究人员能够模拟这些疾病的共同病理特征,观察和分析它们之间的相互作用机制。这不仅有助于我们更普遍地理解肺纤维化的复杂性,还能够揭示肺纤维化与其他肺部疾病之间的潜在联系,为制定综合性的治疗方案提供科学依据。因此,肺纤维化模型在研究肺纤维化与其他肺部疾病关系方面具有不可或缺的价值。科学家通过肺纤维化模型发现了一些新的疾病疗愈靶点。宁夏大鼠肺纤维化模型
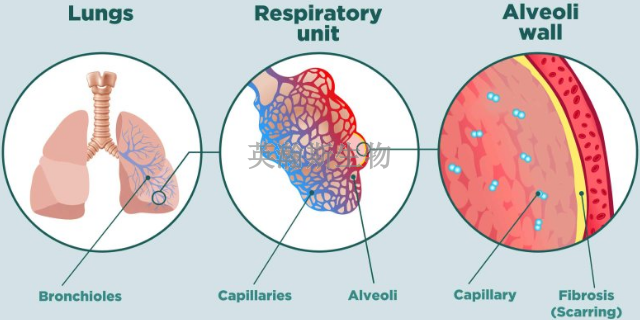
肺纤维化是一种肺部疾病,发生于受损和出现***的肺组织。这种增厚、僵硬的组织使肺更加难以正常运作。随着肺纤维化的恶化,您会逐渐感觉气短。与肺纤维化相关的瘢痕形成可由多种因素引起。但在大多数情况下,医生无法查明问题的根源。如果无法发现原因,就称为特发性肺纤维化。肺纤维化引起的肺损伤无法修复,但药物和疗愈有时可帮助缓解症状和提高生活质量。英瀚斯生物,专业成熟的动物肺纤维化模型构建方法,适用于大鼠、小鼠。已有成功案例。小鼠肺纤维化模型有哪些炎症细胞的浸润是肺纤维化模型中的一个关键步骤。
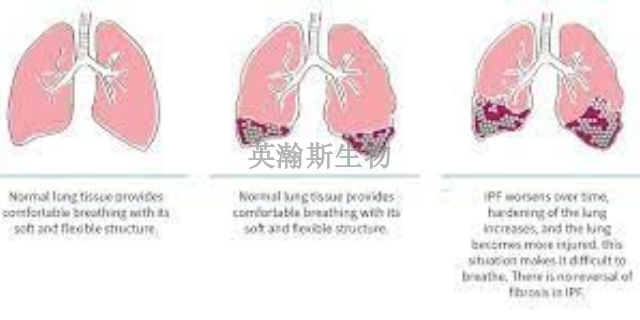
肺纤维化模型为研究人员提供了一个宝贵的平台,使他们能够深入了解肺纤维化的疾病机制。这一模型不仅高度模拟了肺纤维化的病理过程,还展现了疾病发展的多个方面,如炎症细胞的激发、胶原蛋白的沉积以及肺组织结构的改变等。通过这个平台,研究人员可以观察和分析这些变化如何相互作用、影响肺部的功能,并揭示其背后的分子机制。这种深入了解有助于研究人员更好地理解肺纤维化的成因和发展过程,为寻找有效的治疗方法和预防策略提供了坚实的基础。因此,肺纤维化模型在肺纤维化疾病的研究中发挥着不可或缺的作用。
针对不同的研究目的,研究人员需要采用不同的肺纤维化模型。对于***和抗氧化药物的初步筛选,博莱霉素模型的早期炎症阶段(给药后 $3\sim 7$ 天)是理想的平台。若目的是评估药物对肌成纤维细胞***和胶原沉积的抑制作用,则应使用博莱霉素模型的晚期纤维化阶段(给药后 $14\sim 28$ 天)。对于研究疾病慢性进展机制或遗传因素,则应选择遗传突变模型或颗粒物诱导的慢性模型,这些模型需要更长的观察周期,但能提供更接近人类疾病的病理学信息。此外,为了评估新疗法(如细胞疗法或基因疗法)的疗效,有时还需要建立**“***性”模型**,即先诱导纤维化,待纤维化病灶形成后再开始介入***,以模拟临床上对已患病患者的干预,从而证明药物或疗法具有逆转而非**预防纤维化的潜力。博来霉素诱导的纤维化是具特征和经常使用的临床前肺纤维化模型。
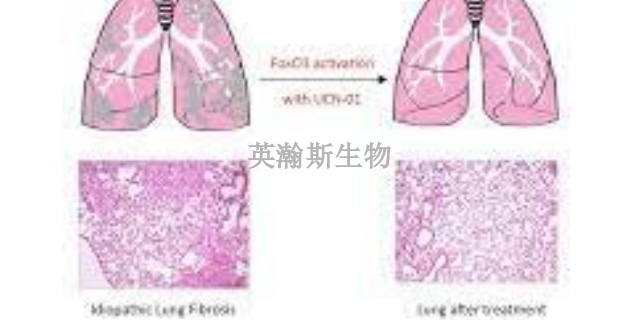
在肺纤维化模型中,肺组织经历了一个复杂而微妙的转变过程,即从炎症逐渐过渡到纤维化。这个过程模拟了人类肺部在遭受长期炎症损伤后,如何逐渐失去其原有的弹性和功能,转而形成坚硬的纤维组织。炎症阶段,肺组织中的免疫细胞被激发,释放出各种炎症介质,导致肺组织受损。随着时间的推移,这些炎症损伤无法得到有效修复,肺组织开始尝试通过纤维化来自我修复,然而这一过程却导致了肺组织的进一步硬化和功能障碍。肺纤维化模型不仅为我们揭示了这一转变的详细过程,也为深入研究肺纤维化的发病机制和治疗方法提供了重要依据。肺纤维化模型为研究人员提供了深入了解疾病机制的平台。甘肃专业的肺纤维化模型造模方法
在肺纤维化模型中,肺纤维化的进程与肺部微环境的改变密切相关。宁夏大鼠肺纤维化模型
除了急性损伤模型外,研究人员还开发了模拟环境或职业暴露导致的慢性肺纤维化模型,其中相当有代表性的是吸入性或灌注性二氧化硅(Silica)模型和吸入性石棉(Asbestos)模型。这些模型通过让动物长期或一次性高剂量暴露于颗粒物,诱发矽肺病或石棉肺,这两种疾病都是由颗粒物引发的慢性炎症和持续性纤维化。二氧化硅颗粒被肺泡巨噬细胞吞噬后,会诱导巨噬细胞凋亡并释放大量促炎症和促纤维化细胞因子(如IL-1 $\beta$ 和TGF-$\beta 1$),从而启动和维持纤维化过程。与博莱霉素模型相比,颗粒物诱导的模型具有更长的潜伏期和更慢的疾病进展速度,更贴近于人类慢性间质性肺病的自然病程,非常适合用于研究疾病的慢性演变过程以及长期干预策略的有效性。然而,这类模型的建模周期长(通常需要 $6$ 周至数月),且结果的异质性较大,对实验操作和环境控制的要求更高。宁夏大鼠肺纤维化模型