- 品牌
- 睿宝和
- 服务项目
- 病理实验 动物实验 免疫实验 实验服务
石蜡切片在进行染色或其他检测之前,需要进行脱蜡与水化操作。这是因为石蜡切片中的石蜡会阻碍后续试剂与组织的接触,必须将其去除并使组织重新水化。脱蜡过程通常使用二甲苯。将石蜡切片放入二甲苯中,二甲苯会溶解石蜡,一般需要浸泡两次,每次5-10分钟。脱蜡后的切片要经过梯度乙醇溶液进行水化,从高浓度乙醇逐步过渡到低浓度乙醇,***到水。例如,先在100%乙醇中浸泡1-2分钟,然后在95%乙醇、80%乙醇、70%乙醇中各浸泡1分钟,***浸泡在水中。这个过程要注意操作的连贯性,如果在脱蜡过程中二甲苯未完全去除,可能会影响后续的水化效果,进而影响染色等操作。同样,在水化过程中,如果梯度乙醇过渡不自然,可能会导致组织收缩或膨胀,影响切片的质量。脱蜡与水化后的切片就可以进行如HE染色、免疫组织化学染色等后续操作了。动物实验有助于研究动物的生物化学和分子生物学特征,为生物技术和基因工程提供数据支持。河北细胞实验作品

药物的鉴别实验是确定药物真伪的重要手段。不同类型的药物采用不同的鉴别方法。对于化学药物,化学鉴别法是常用的方法之一。例如,利用药物与特定试剂发生的化学反应产生的颜色、沉淀或气体等现象进行鉴别。以氯化物药物为例,可利用硝酸银试剂与其反应,产生白色沉淀(氯化银),且沉淀不溶于稀硝酸,从而鉴别药物中是否含有氯化物。光谱鉴别法在药物鉴别中也具有重要地位。紫外-可见分光光度法通过测定药物在特定波长下的吸收光谱来鉴别药物。不同的药物具有不同的分子结构,其吸收光谱具有特征性。例如,对乙酰氨基酚在257nm波长处有比较大吸收峰,通过与标准品的吸收光谱对比,可以鉴别该药物。红外光谱法是一种更为精确的鉴别方法。药物分子在红外光区的吸收会产生特定的红外吸收光谱,这一光谱就像药物的“指纹”一样。将待测药物的红外光谱与标准图谱进行比对,如果两者一致,则可确定药物的真伪。这种方法对于结构复杂的药物鉴别尤为有效。此外,对于生物制品等特殊药物,还可能采用免疫学法、电泳法等特殊的鉴别方法。宁波实验作品动物实验还可以帮助我们了解动物的传染和免疫机制,为传染病和免疫学研究提供重要的实验数据。

药理实验中研究药物对凝血功能的影响对于开发抗凝血或促凝血药物意义重大。实验常用家兔或大鼠等动物。可以通过多种方法检测凝血功能。一种是测定凝血时间,例如,采用玻片法或试管法。在玻片法中,刺破动物的耳垂或指尖取血,滴在玻片上,同时开始计时,观察血液凝固所需时间;试管法是将血液采集到试管中,倾斜试管观察血液不再流动的时间。将动物随机分组后,给予不同剂量的待测药物。然后检测给药后的凝血时间。如果药物使凝血时间延长,可能是抗凝血药物,如肝素通过增强抗凝血酶III的活性来抑制凝血过程;反之,如果凝血时间缩短,则可能是促凝血药物,如维生素K参与凝血因子的合成从而促进凝血。此外,还可以检测血液中的凝血因子活性、血小板功能等指标,更***地评估药物对凝血功能的影响,这有助于在心血管疾病(如血栓形成、出血性疾病等)的***中合理应用药物。
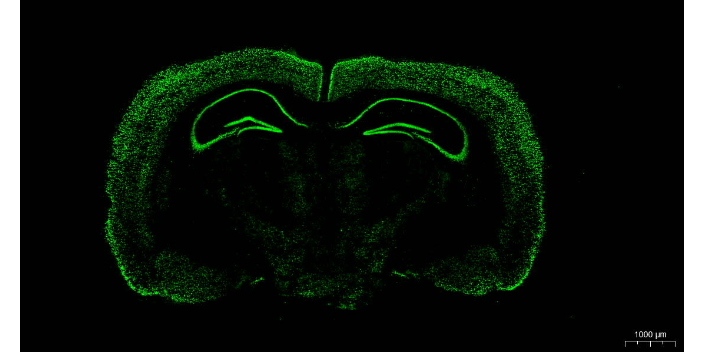
免疫荧光染色是病理实验中一种重要的检测技术。它基于抗原-抗体特异性结合原理,与免疫组织化学染色类似,但标记物为荧光素。首先,组织切片或细胞涂片要进行固定、通透处理,使抗体能够进入细胞内与抗原结合。然后将切片与一抗孵育,一抗与目标抗原特异性结合。孵育后洗涤切片,再与带有荧光标记的二抗孵育。常用的荧光素有异硫氰酸荧光素(FITC),发出绿色荧光;四甲基罗丹明异硫氰酸酯(TRITC),发出红色荧光等。在荧光显微镜下,可以观察到带有荧光标记的抗原分布情况。病理实验可以帮助医生和科研人员了解疾病的类型、程度和预后,为临床诊断和医疗提供依据。

药物对肝药酶的影响实验对于理解药物相互作用和药物安全性至关重要。常用大鼠或小鼠作为实验动物。肝药酶在药物的代谢过程中起着关键作用,例如细胞色素P450酶系。首先,要确定动物体内肝药酶的基础活性。可以通过特定的底物-产物反应来测定,如使用特定的药物作为底物,检测其代谢产物的生成速度。将动物随机分组,给予待测药物,然后在一定时间后再次测定肝药酶的活性。如果药物使肝药酶活性增强,可能会加快其他药物的代谢,导致其他药物疗效降低;反之,如果使肝药酶活性降低,则可能使其他药物在体内的浓度升高,增加药物中毒的风险。例如,某些药物(如利福平)是肝药酶诱导剂,而另一些药物(如酮康唑)是肝药酶抑制剂。这个实验有助于预测药物在体内的相互作用,为临床合理用药提供指导,避免因药物相互作用而产生的不良反应。病理实验还可以通过分子遗传学技术,研究疾病相关基因的突变和表达变化,揭示疾病的遗传基础。河北细胞实验作品
动物实验可以帮助我们了解动物的行为和社会结构,为动物行为学和社会学研究提供数据支持。河北细胞实验作品
药物的稳定性实验对于确保药品的质量和疗效至关重要。稳定性实验包括影响因素实验、加速实验和长期实验。影响因素实验主要研究药物在高温、高湿、强光等极端条件下的稳定性。例如,将药物样品分别置于高温(如60°C)、高湿(相对湿度90%以上)和强光(4500lx)环境中,在规定的时间内(如10天)定期取样,检测药物的外观、含量、有关物质等指标的变化。加速实验则是在超常的储存条件下,预测药物的稳定性。一般采用温度40°C±2°C、相对湿度75%±5%的条件,对药物进行6个月的实验。通过定期取样检测,利用动力学原理来推算药物在常温下的有效期。长期实验是在接近药物实际储存条件下进行的实验。例如,将药物置于温度25°C±2°C、相对湿度60%±10%的环境中,持续2-3年甚至更长时间,观察药物的各项质量指标的变化。这个实验能够真实反映药物在储存过程中的稳定性,为药品的有效期确定、包装材料选择和储存条件的制定提供依据。河北细胞实验作品
药物的半数致死量(LD50)是衡量药物毒性的重要指标。在这个实验中,通常选用小白鼠等实验动物。首先,要将动物随机分组,每组若干只,一般不少于6组。然后,给予不同剂量的药物。剂量的设置要有一定的梯度,从低剂量开始逐渐增加。药物的给予途径可以是口服、腹腔注射、静脉注射等,这取决于药物的性质和实验目的。给药后,观察动物在一段时间内(通常为24-48小时)的死亡情况。通过统计分析,计算出能够使50%的实验动物死亡的药物剂量,即LD50。LD50数值越小,说明药物的毒性越大。这个实验有助于初步评估药物的安全性,为后续的药物研发和临床应用提供重要的参考。例如,在开发新的***药物时,虽然期望药物对*细胞有...
- 济南医学动物实验记录 2024-12-06
- 济南动物实验计划 2024-12-06
- 山东超微病理实验有哪些 2024-12-05
- 上海分子实验记录 2024-12-04
- 青岛医学动物实验步骤 2024-12-04
- 石家庄科学实验服务 2024-12-04
- 青岛病理实验设计 2024-12-04
- 杭州动物细胞实验步骤 2024-12-04
- 南京动物实验器材 2024-12-04
- 济南分子实验作品 2024-12-04